Les chercheurs ont développé une nouvelle version d'une protéine clé d'édition de gènes CRISPR qui présente une activité d'édition efficace et est suffisamment petite pour être intégrée dans un virus non pathogène capable de la transmettre aux cellules cibles. Hongjian Wang et ses collègues de l'Université de Wuhan, en Chine, présentent ces résultats dans la revue en libre accès PLOS Biology.
Ces dernières années ont vu une explosion de recherches tentant d’exploiter les systèmes d’édition de gènes CRISPR – que l’on trouve naturellement dans de nombreuses bactéries comme moyen de défense contre les virus – afin qu’ils puissent être utilisés comme traitements potentiels pour les maladies humaines. Ces systèmes s'appuient sur des protéines dites associées à CRISPR (Cas), Cas9 et Cas12a étant les deux types les plus largement utilisés, chacun avec ses propres particularités et forces.
Une idée prometteuse consiste à intégrer les protéines CRISPR dans un virus non pathogène, qui pourrait ensuite délivrer les protéines aux cellules cibles; là, ils modifieraient des séquences d’ADN spécifiquement ciblées pour traiter la maladie. Cependant, le virus adéno-associé couramment utilisé est petit et, même si certaines protéines Cas9 peuvent s'y glisser, les protéines Cas12a sont généralement trop grosses.
Maintenant, Wang et ses collègues ont identifié une version relativement petite de Cas12a, appelée EbCas12a, qui se produit naturellement chez une espèce de la classe de bactéries Erysipelotrichia. En remplaçant délibérément l'un des éléments constitutifs des acides aminés de la protéine par un autre, ils ont amélioré son efficacité en matière d'édition génétique.
Lorsqu'elle est appliquée à des cellules de mammifères dans une boîte en laboratoire, cette protéine modifiée, baptisée enEbCas12a, présente une efficacité d'édition génétique comparable à celle de deux autres protéines Cas12a connues pour leur édition génétique très précise.
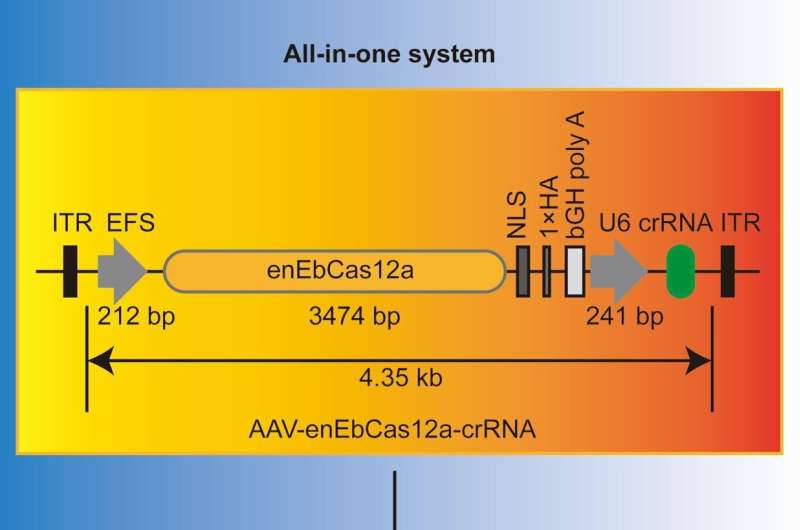
L’équipe de recherche a ensuite démontré qu’enEbCas12a est suffisamment petit pour être utilisé pour la thérapie génique à base de virus adéno-associés. Ils ont modifié enEbCas12a pour cibler un gène spécifique associé au cholestérol, l'ont intégré au virus et ont administré le virus à des souris ayant un taux de cholestérol élevé. Un mois plus tard, ils ont constaté une réduction significative du taux de cholestérol sanguin chez les souris traitées, par rapport aux souris n'ayant pas reçu le virus.
Des recherches supplémentaires seront nécessaires pour déterminer si enEbCas12a pourrait un jour être utilisé pour lutter contre les maladies humaines. Néanmoins, ces résultats suggèrent qu'il pourrait être possible d'utiliser un virus adéno-associé pour délivrer des protéines Cas12a à des fins de thérapie génique.
Les auteurs ajoutent :« Le nouveau compact enEbCas12a, ainsi que son crRNA, peuvent être intégrés dans un système AAV tout-en-un pour une édition génétique pratique in vitro et in vivo avec une haute fidélité, ce qui peut être très bénéfique pour de futures applications cliniques. et d'autres développements d'outils, notamment l'édition multigène tout-en-un basée sur l'AAV, l'édition de base, l'édition d'amorces, etc."