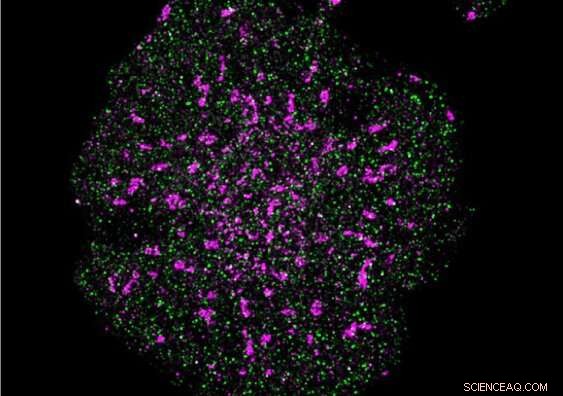
Une cellule T avec une localisation précise des récepteurs des cellules T (rose) et de la phosphatase CD45 (vert). Crédit :Science de la molécule unique
Un microscope ultra-précis qui dépasse les limites de la microscopie à super-résolution lauréate du prix Nobel permettra aux scientifiques de mesurer directement les distances entre les molécules individuelles.
Les chercheurs médicaux de l'UNSW ont atteint des capacités de résolution sans précédent en microscopie à molécule unique pour détecter les interactions entre des molécules individuelles au sein de cellules intactes.
Le prix Nobel de chimie 2014 a été décerné pour le développement d'une technologie de microscopie à fluorescence à super-résolution qui a permis aux microscopistes d'avoir la première vue moléculaire à l'intérieur des cellules, une capacité qui a fourni de nouvelles perspectives moléculaires sur des systèmes et processus biologiques complexes.
Aujourd'hui, la limite de détection des microscopes à molécule unique est à nouveau dépassée, et les détails sont publiés dans le numéro actuel de Avancées scientifiques .
Alors que des molécules individuelles pouvaient déjà être observées et suivies par microscopie à super-résolution, les interactions entre ces molécules se produisent à une échelle au moins quatre fois plus petite que celle résolue par les microscopes à molécule unique existants.
"La raison pour laquelle la précision de localisation des microscopes à molécule unique est d'environ 20-30 nanomètres est normalement parce que le microscope se déplace réellement pendant que nous détectons ce signal. Cela conduit à une incertitude. Avec les instruments de super-résolution existants, nous ne pouvons pas dire si une protéine est liée ou non à une autre protéine car la distance entre elles est plus courte que l'incertitude de leurs positions, " déclare Katharina Gaus, professeure de Scientia, chef d'équipe de recherche et chef du nœud australien EMBL de l'UNSW Medicine en science des molécules uniques.
Pour contourner ce problème, l'équipe a construit des boucles de rétroaction autonomes à l'intérieur d'un microscope à molécule unique qui détecte et réaligne le chemin optique et la scène.
"Peu importe ce que vous faites à ce microscope, il retrouve fondamentalement son chemin avec une précision inférieure au nanomètre. C'est un microscope intelligent. Il fait tout ce qu'un opérateur ou un ingénieur de service doit faire, et il le fait 12 fois par seconde, " dit le professeur Gaus.
Mesurer la distance entre les protéines
Avec la conception et les méthodes décrites dans le document, le système de rétroaction conçu par l'équipe UNSW est compatible avec les microscopes existants et offre une flexibilité maximale pour la préparation des échantillons.
"C'est une solution vraiment simple et élégante à un problème d'imagerie majeur. Nous venons de construire un microscope dans un microscope, et tout ce qu'il fait, c'est aligner le microscope principal. Que la solution que nous avons trouvée soit simple et pratique est une vraie force car elle permettrait un clonage facile du système, et l'adoption rapide de la nouvelle technologie, " dit le professeur Gaus.
Pour démontrer l'utilité de leur microscope monomoléculaire à rétroaction ultra-précis, les chercheurs l'ont utilisé pour effectuer des mesures de distance directes entre les protéines de signalisation dans les cellules T. Une hypothèse populaire en immunologie cellulaire est que ces cellules immunitaires restent dans un état de repos lorsque le récepteur des cellules T est à côté d'une autre molécule qui agit comme un frein.
Leur microscope de haute précision a pu montrer que ces deux molécules de signalisation sont en fait davantage séparées l'une de l'autre dans les cellules T activées, relâcher le frein et activer la signalisation des récepteurs des cellules T.
"Les techniques de microscopie conventionnelles ne seraient pas en mesure de mesurer avec précision un si petit changement, car la distance entre ces molécules de signalisation dans les cellules T au repos et dans les cellules T activées ne différait que de 4 à 7 nanomètres, " dit le professeur Gaus.
"Cela montre également à quel point ces machineries de signalisation sont sensibles à la ségrégation spatiale. Afin d'identifier des processus de régulation comme ceux-ci, nous devons effectuer des mesures de distance précises, et c'est ce que permet ce microscope. Ces résultats illustrent le potentiel de cette technologie pour des découvertes qui ne pourraient être faites par aucun autre moyen. »
Chercheur postdoctoral, Dr Simao Pereira Coelho, avec Ph.D. l'étudiant Jongho Baek, qui a depuis obtenu son doctorat. degré - a dirigé la conception, développement, et la construction de ce système. Le Dr Baek a également reçu le prix du doyen pour un doctorat exceptionnel. Thèse pour ce travail.