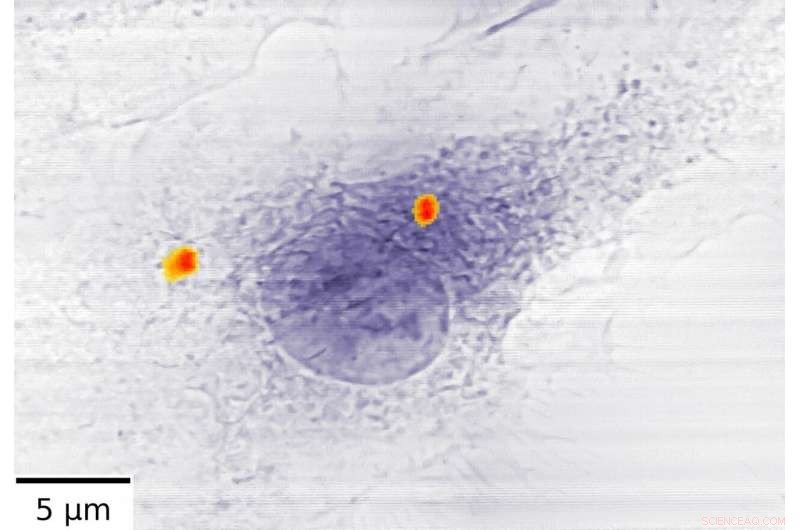
Deux agglomérats de nanoconteneurs de fer chargés d'antibiotiques (rouge) dans un macrophage. Crédit :Stachnik et al., Rapports scientifiques , DOI :10.1038/s41598-020-58318-7, CC BY 4.0
Avec une technique avancée de combinaison de rayons X, les scientifiques ont tracé des nanosupports pour les médicaments antituberculeux dans les cellules avec une très grande précision. La méthode combine deux mesures sophistiquées aux rayons X à balayage et peut localiser des quantités infimes de divers métaux dans des échantillons biologiques à très haute résolution, en équipe autour de la scientifique de DESY, Karolina Stachnik, rapporte dans la revue Rapports scientifiques . Pour illustrer sa polyvalence, les chercheurs ont également utilisé la méthode combinée pour cartographier la teneur en calcium dans les os humains, une analyse qui peut profiter à la recherche sur l'ostéoporose.
« Les métaux jouent un rôle clé dans de nombreux processus biologiques, du transport de l'oxygène dans nos globules rouges et de la minéralisation des os à l'accumulation préjudiciable de métaux dans les cellules nerveuses comme on le voit dans des maladies comme la maladie d'Alzheimer, " explique Stachnik qui travaille au Centre de science des lasers à électrons libres (CFEL) à DESY. Les rayons X à haute énergie font s'illuminer les métaux en fluorescence, une méthode qui est très sensible même à de petites quantités. "Toutefois, les mesures de fluorescence X ne montrent généralement pas l'ultrastructure d'une cellule, par exemple, " déclare le scientifique de DESY, Alke Meents, qui a dirigé la recherche. " Si vous voulez localiser exactement les métaux dans votre échantillon, il faut combiner les mesures avec une technique d'imagerie. » L'ultrastructure comprend les détails de la morphologie cellulaire qui ne sont pas visibles au microscope optique.
En tant qu'échantillons biologiques, comme les cellules, sont très sensibles aux rayons X, il est très avantageux d'imager leur structure simultanément à l'analyse de fluorescence. Pour cette raison, l'équipe a combiné les mesures de fluorescence avec une méthode d'imagerie connue sous le nom de ptychographie. "Un microscope ptychographique est assez similaire à la prise d'une image panoramique, " explique Stachnik. " Un spécimen étendu comme une cellule biologique est balayé par trame avec un petit faisceau de rayons X cohérent qui produit de nombreuses images superposées de parties de l'échantillon. Ces images qui se chevauchent sont ensuite assemblées par la suite."
La méthode appliquée fonctionne sans lentilles entre l'échantillon et le détecteur, et par conséquent, ce que l'on appelle des diagrammes de diffraction des rayons X sont enregistrés sur le détecteur. Chacun de ces modèles contient des informations sur la structure spatiale de la partie respective de l'échantillon, qui peut être calculé à partir du modèle. "Cela aboutit finalement à une carte de densité optique entièrement quantitative de l'échantillon, " explique Stachnik. " Par ce processus complexe, La ptychographie fournit des résolutions spatiales au-delà des limites habituelles de l'optique à rayons X."
Grâce à sa nature de numérisation, La ptychographie peut être combinée à l'acquisition simultanée de mesures de fluorescence X qui fournissent une empreinte unique des éléments constituant l'échantillon. De cette façon, une photographie de la morphologie de l'échantillon obtenue par ptychographie peut être superposée à une carte des éléments. "La combinaison simultanée de ces deux méthodes d'imagerie complémentaires permet donc des corrélations sans artefact d'éléments traces avec la structure de l'échantillon hautement résolu, " résume Meents.
Un préalable fondamental est que les rayons X soient d'une seule couleur (monochromatique, ayant tous la même longueur d'onde) et qu'ils oscillent en pas (cohérent) comme dans un laser. « Des rayons X monochromatiques cohérents suffisamment brillants avec des énergies suffisamment élevées pour permettre la fluorescence de métaux comme le fer ne sont devenus disponibles que dans des sources de lumière synchrotron modernes comme PETRA III de DESY, " dit Meents.
Pour tester la méthode, les chercheurs de DESY se sont associés au groupe d'Ulrich Schaible du Centre de Recherche de Borstel pour étudier la localisation et la concentration de nanotransporteurs de médicaments antituberculeux au sein des macrophages, les cellules charognardes du système immunitaire. "D'habitude, les macrophages détruisent les agents pathogènes comme les virus et les bactéries. Malheureusement, les bactéries de la tuberculose ont réussi à échapper à la destruction et à se cacher à l'intérieur des macrophages, même les utiliser pour grandir, " dit Schaible. " En tant que barrière à un traitement efficace, les niches des bactéries au sein des macrophages doivent être atteintes par des antibiotiques pour être efficaces."
Une nouvelle stratégie de « Cheval de Troie » utilise des conteneurs en fer de taille nanométrique pour administrer des antibiotiques directement dans les cellules. Ces récipients sont creux, rempli d'antibiotiques et mesure moins de 20 nanomètres de diamètre (un nanomètre est un millionième de millimètre). "Les macrophages avalent les contenants, et une fois à l'intérieur de la cellule, les parois de fer des cages se dissolvent lentement en raison du besoin des bactéries en fer. Finalement, les antibiotiques sont libérés et tuent les bactéries, " explique Schaible.
Pour évaluer l'efficacité de cette stratégie, l'équipe a étudié les macrophages qui avaient été nourris avec des récipients en fer. En utilisant une platine de balayage spécialement développée sur la ligne de lumière de bio-imagerie et de diffraction P11 de la source de rayons X PETRA III de DESY, les chercheurs ont pu capturer des images ptychographiques et de fluorescence de 14 cellules avec une résolution subcellulaire et ont identifié un total de 22 agglomérats de nanoconteneurs en leur sein.
Dans une deuxième application, les chercheurs se sont associés au groupe de Björn Busse du Centre médical universitaire de Hambourg-Eppendorf (UKE) et ont analysé la teneur en calcium d'un échantillon d'os humain. « Le calcium est un élément clé qui renforce nos os, " explique la co-auteure Katharina Jähn du groupe de Busse. " Cependant, en période de besoin élevé en calcium, le corps le dissout des os pour être utilisé ailleurs. Ces processus et d'autres liés à l'âge peuvent conduire à l'ostéoporose, affectant près d'un quart de toutes les femmes de plus de 50 ans en Allemagne."
La recherche expérimentale sur la minéralisation osseuse est généralement effectuée sur de petites tranches d'os. "Toutefois, seule la teneur totale en calcium est généralement cartographiée de cette façon, " dit Stachnik. " Pour obtenir une véritable mesure de la concentration de calcium, il faut corriger l'épaisseur souvent variable de l'échantillon. » L'équipe a utilisé une image ptychographique obtenue simultanément pour supprimer la distorsion masse-épaisseur de la carte de distribution du calcium. « Avec cette approche, nous avons pu observer une teneur en calcium localement inférieure à certains points de l'os, qui permet de mieux comprendre le processus des troubles osseux et de quantifier l'effet des modifications de la minéralisation osseuse chez les patients, " souligne Stachnik.
Pour améliorer encore la méthode, les chercheurs ont commencé à étendre l'analyse aux mesures tridimensionnelles. « Le dispositif expérimental est actuellement en cours d'extension pour permettre l'acquisition de jeux de données tomographiques 3D sur la ligne de lumière P11, " dit Meents. " Avec de nombreux synchrotrons mis à niveau pour produire des rayons X encore plus brillants, nous nous attendons à ce que la méthode augmente le débit et devienne une application de routine dans ces installations. »
Le Centre de Recherche Borstel, l'Institut Paul Scherrer en Suisse, l'Institut de technologie de Karlsruhe, le Centre médical universitaire de Hambourg-Eppendorf et DESY ont été impliqués dans cette recherche.
DESY est l'un des principaux centres d'accélérateurs de particules au monde et étudie la structure et la fonction de la matière, de l'interaction de minuscules particules élémentaires et le comportement de nouveaux nanomatériaux et biomolécules vitales aux grands mystères de l'univers. Les accélérateurs et détecteurs de particules que DESY développe et construit sur ses sites de Hambourg et de Zeuthen sont des outils de recherche uniques. Ils génèrent le rayonnement X le plus intense au monde, accélérer les particules pour enregistrer les énergies et ouvrir de nouvelles fenêtres sur l'univers. DESY est membre de l'Association Helmholtz, La plus grande association scientifique d'Allemagne, et reçoit son financement du ministère fédéral allemand de l'éducation et de la recherche (BMBF, 90 pour cent) et les Länder allemands de Hambourg et de Brandebourg (10 pour cent).