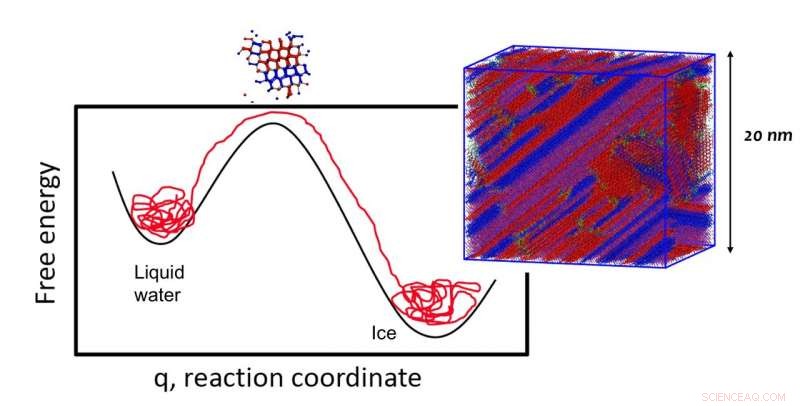
Un diagramme de la barrière d'énergie libre représente l'énergie nécessaire pour maintenir la nucléation de la glace, avec un petit diagramme d'une cristallite suffisamment dimensionnée au sommet de la barrière. Un modèle à plus grande échelle (à droite) montre un segment cubique d'une plus grande cristallite, avec des molécules empilées cubiquement en rouge et des molécules empilées hexagonalement en bleu. Crédit :Université de l'Utah
Quelque chose de presque magique se produit lorsque vous mettez un plateau plein de clapotis, l'eau liquide dans un congélateur et elle sort plus tard sous forme de rigide, cristal de glace solide. Les chimistes de l'Université de l'Utah ont levé un peu plus le rideau sur le processus de congélation, en particulier dans les nuages.
Leurs recherches montrent que lorsque les gouttelettes d'eau gèlent dans les nuages, la structure du cristal de glace n'est pas nécessairement la structure classique du flocon de neige hexagonal. Plutôt, une structure de glace plus désordonnée se forme plus facilement que la glace hexagonale dans certaines conditions nuageuses, permettant aux gouttelettes d'eau dans les nuages de se transformer en glace plus rapidement que prévu. Le travail réconcilie des modèles théoriques de nuages avec des observations de taux de congélation. L'étude est publiée dans La nature .
Pourquoi l'eau gèle
Même dans les climats chauds, les précipitations commencent généralement par des gouttelettes d'eau dans les nuages qui se transforment en glace. Pourquoi? "Ces gouttelettes de liquide peuvent atteindre une certaine taille, " dit Valeria Molinero, professeur de chimie à l'Université de l'Utah, "mais pour atteindre une taille suffisamment grande pour qu'elle puisse tomber du ciel, ces gouttelettes doivent devenir beaucoup plus grosses."
La meilleure façon de grossir est de se tourner vers la glace. Une petite particule atmosphérique, appelé aérosol, peut démarrer le processus de congélation dans l'eau réfrigérée. Ou le processus peut démarrer spontanément, avec une petite région de molécules d'eau ordonnées apparaissant dans la gouttelette. Si ce "cristallite" est assez gros, alors la gouttelette peut geler et continuer à croître en attirant la vapeur d'eau environnante. Le processus de croissance des cristaux à partir d'un petit noyau est appelé nucléation.
Surmonter la barrière
Les petits noyaux cristallins sont confrontés à un obstacle à la croissance. En raison des interactions entre un petit solide et son environnement liquide, une cristallite doit atteindre une certaine taille pour pouvoir continuer à croître et ne pas simplement fondre. Imaginez une colline. Si vous poussez un rocher en haut d'une colline mais que vous n'atteignez pas le sommet, le rocher redescend à l'endroit où vous avez commencé. Mais si tu pousses assez loin, il roule de l'autre côté. Le sommet de la colline (appelée barrière d'énergie libre) définit la taille critique pour continuer à faire croître la cristallite.
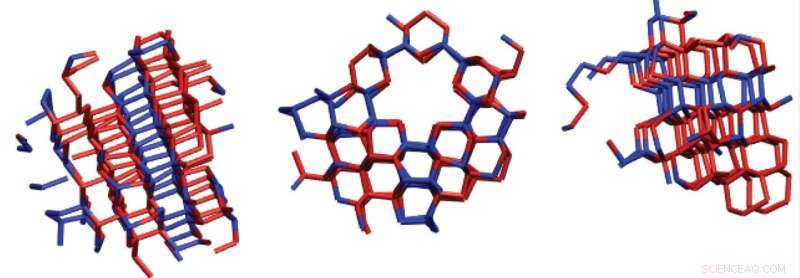
Noyaux de glace avec une cubicité et une taille suffisantes pour continuer la formation de glace. Les molécules rouges affichent une configuration moléculaire cubique et les molécules bleues sont dans un ordre de glace hexagonal. Crédit :Université de l'Utah
"L'objectif de notre article est de montrer quelle est la structure de la cristallite au sommet de cette barrière et quelle est l'implication pour le taux de nucléation, " dit Molinero.
Précédemment, les chimistes ont supposé que la structure de la glace au sommet de la barrière énergétique était la structure hexagonale observée dans les flocons de neige (bien que les flocons de neige soient beaucoup plus gros que les cristallites). C'est une structure très stable. "L'hypothèse qu'elle est hexagonale est la plus intuitive, " dit Laura Lupi, chercheur postdoctoral et premier auteur sur le La nature papier.
Gâteau étagé en pêle-mêle
Des simulations précédentes ont montré que dans certaines conditions nuageuses, cependant, les cristallites avec une structure désordonnée étaient plus favorisées. Ces structures « empilées désordonnées » sont un mélange de molécules en couches qui ne se déposent pas dans la structure cristalline hexagonale ou cubique. Dans leur étude, Lupi et Molinero ont découvert qu'à une température de 230 K, ou -45 degrés Farenheit, la barrière d'énergie libre pour la cristallite désordonnée d'empilement est inférieure de 14 kJ/mol à celle de la glace hexagonale. En d'autres termes, la glace désordonnée a une "colline" beaucoup plus petite que la glace hexagonale et se forme autour de 2, 000 fois plus rapide.
Cela aide les modélisateurs de nuages à mieux comprendre leurs données d'observation concernant les taux de gel dans les nuages. Les modèles de nucléation précédents utilisant de la glace hexagonale ne pouvaient pas capturer tout le comportement d'un nuage, car ces modèles extrapolaient les taux de nucléation à travers les températures des nuages sans comprendre les effets de la température sur ces taux. L'étude de Lupi et Molinero commence à corriger ces modèles. « Les taux de nucléation de la glace ne peuvent être mesurés que dans une plage de températures très étroite, " Molinero dit, "et il est extrêmement difficile de les extrapoler à des températures plus basses qui sont importantes pour les nuages mais inaccessibles aux expériences."
De par leur taille, les flocons de neige sont plus stables que la glace hexagonale, Lupi et Molinero disent. Leurs découvertes ne s'appliquent qu'aux très petites cristallites. Lupi dit que leur travail peut aider les modélisateurs de nuages à créer des modèles plus précis de la phase de l'eau dans les nuages. "Si vous avez autant de gouttelettes d'eau à une certaine température, vous voulez prédire combien se transformeront en gouttelettes de glace, " dit-elle. De meilleurs modèles de nuages peuvent conduire à une meilleure compréhension de la façon dont les nuages réfléchissent la chaleur et produisent des précipitations.
Molinero dit que leur travail améliore la compréhension fondamentale de la rapidité avec laquelle l'eau forme de la glace - un processus qui se déroule chaque jour dans les nuages et les congélateurs. Et c'est un processus, pas un événement instantané, Molinero ajoute. "La transformation n'est pas seulement que vous descendez en dessous de zéro et c'est tout, " dit-elle. " Il y a un rythme auquel la transition se produit, contrôlé par la barrière de nucléation. Et la barrière est plus basse que prévu."