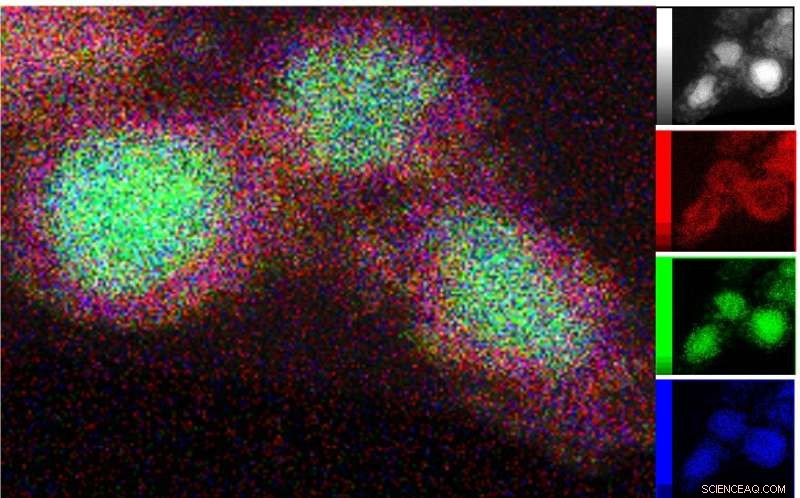
La microscopie électronique à transmission (TEM) de la phase catalytiquement active a été combinée à la spectroscopie à rayons X à dispersion d'énergie pour cartographier la distribution de Ni (vert), Si (bleu) et d'oxygène (rouge) autour des structures noyau-coque. Crédit :P. Menezes /HZB/TU Berlin
L'électrolyse est peut-être un concept familier des cours de chimie à l'école :deux électrodes sont immergées dans l'eau et mises sous tension. Cette tension provoque la décomposition des molécules d'eau en leurs composants et des bulles de gaz montent au niveau des électrodes :de l'oxygène gazeux se forme à l'anode, tandis que des bulles d'hydrogène se forment à la cathode. L'électrolyse pourrait produire de l'hydrogène dans un CO2 - de manière neutre - tant que l'électricité requise est générée par des formes d'énergie non fossiles telles que le soleil ou le vent.
Le seul problème est que ces réactions ne sont pas très efficaces et extrêmement lentes. Pour accélérer les réactions, on utilise des catalyseurs, à base de métaux précieux et rares comme le platine, le ruthénium ou l'iridium. Pour une utilisation à grande échelle, cependant, ces catalyseurs doivent être constitués d'éléments largement disponibles et très bon marché.
Nanostructures induites chimiquement
Pour accélérer la réaction de dégagement d'oxygène à l'anode, les matériaux à base de nickel sont considérés comme de bons candidats. Le nickel est résistant à la corrosion, peu toxique et également peu coûteux. Jusqu'à présent, cependant, les procédés à haute température énergivores ont été principalement utilisés pour produire des matériaux catalyseurs à base de nickel.
Une équipe dirigée par le Dr Prashanth Menezes (HZB/TU Berlin) a maintenant trouvé un moyen "chimique doux" de produire un catalyseur efficace à base de nanocristaux intermétalliques de nickel-silicium.
"Nous avons combiné l'élément nickel avec le silicium, le deuxième élément le plus abondant de la croûte terrestre, et avons réalisé une nanostructuration via une réaction chimique. Le matériau résultant possède d'excellentes propriétés catalytiques", explique Menezes. Le Ni2 cristallin Si a servi de précatalyseur pour la réaction de dégagement d'oxygène alcalin à l'anode et subit une transformation de surface pour former du nickel (oxy) hydroxyde en tant que catalyseur actif dans des conditions de fonctionnement. Remarquablement, l'électrolyse de l'eau a été en outre associée à une réaction d'oxydation organique à valeur ajoutée dans laquelle l'électrosynthèse de composés nitriles de valeur industrielle a été produite à partir d'amines primaires avec une conversion sélective et complète dans des conditions douces. De telles méthodes électrosynthétiques peuvent stimuler la génération d'hydrogène à la cathode et peuvent simultanément donner accès à des produits industriels de valeur à l'anode.
Plus efficace et stable
Comparé aux catalyseurs modernes à base de Nickel, Cobalt, Fer, Ruthénium et Iridium, le Ni2 nanoporeux Si est significativement plus actif et reste stable pendant un temps de réaction plus long dans des conditions de niveau industriel. Comprendre le comportement du Ni2 Si plus en détail, l'équipe a combiné différentes méthodes de mesure, y compris les analyses élémentaires, la microscopie électronique et les mesures spectroscopiques modernes à BESSY II. "A l'avenir, même les électrolyseurs d'eau alcalins industriels pourraient être équipés d'un revêtement de ce siliciure de nickel nanoporeux", déclare Menezes.
La recherche a été publiée dans Advanced Energy Materials . Le nickel recouvert de carbone permet une pile à combustible à hydrogène sans métaux précieux