
Pliez votre propre nanocube ! Bien que les nanocubes utilisés dans le projet de recherche se construisent eux-mêmes, vous pouvez plier le vôtre en utilisant ce modèle. Chaque X jaune représente les emplacements où les chercheurs de l'Université de Tokyo ont utilisé différents atomes avec différents niveaux de polarisabilité. Crédit :Shuichi Hiraoka, CC-BY-ND
Le processus de construction d'un petit cube a révélé certains des mystères fondamentaux de la façon dont les molécules se lient dans les environnements naturels. Les chercheurs espèrent appliquer ces connaissances à de futurs projets de conception de structures complexes pouvant imiter la vie.
Lorsque deux molécules entourées d'eau se rapprochent, une partie de leur attraction initiale est parfois due à la force chimique pour repousser l'eau - l'effet hydrophobe.
Une fois les molécules proches les unes des autres, mais pas encore formellement lié, une force beaucoup plus faible devient importante :la force de dispersion.
"Notre rêve est de contrôler la force de dispersion et de fournir un principe de conception simple pour utiliser la force de dispersion pour construire des structures d'auto-assemblage complexes, " a déclaré le professeur Shuichi Hiraoka, chef du laboratoire où la recherche a été effectuée dans le département des sciences fondamentales de l'Université de Tokyo.
Les forces de dispersion sont un type de forces de van der Waals, certaines des interactions chimiques les plus faibles connues dans la nature. Bien que faible, les forces de van der Waals sont importantes; ils aident les geckos à gravir les murs et ont déjà été identifiés en 2018 par le même groupe de recherche comme verrouillant ensemble les molécules en forme d'engrenage ou de flocon de neige des nanocubes auto-assemblés.
Mesurer la force de dispersion dans des conditions naturelles, comme lorsque les molécules sont en solution avec de l'eau, a été impossible. La force est si faible qu'elle ne peut pas être identifiée séparément des autres forces en jeu.
Cependant, dans de nouvelles expériences, l'équipe de recherche a utilisé ses nanocubes auto-assemblés comme outils pour amplifier les différences de force de dispersion.
Les molécules qui composent les côtés des cubes ont été modifiées pour contenir des atomes sélectionnés pour leur polarisabilité, ce qui signifie leur réactivité au champ électrique environnant. Chaque nanocube entièrement assemblé contenait 18 de ces atomes polarisables.
L'effet combiné de 18 atomes était suffisant pour créer des différences mesurables dans la force de dispersion en fonction de l'atome polarisable attaché.
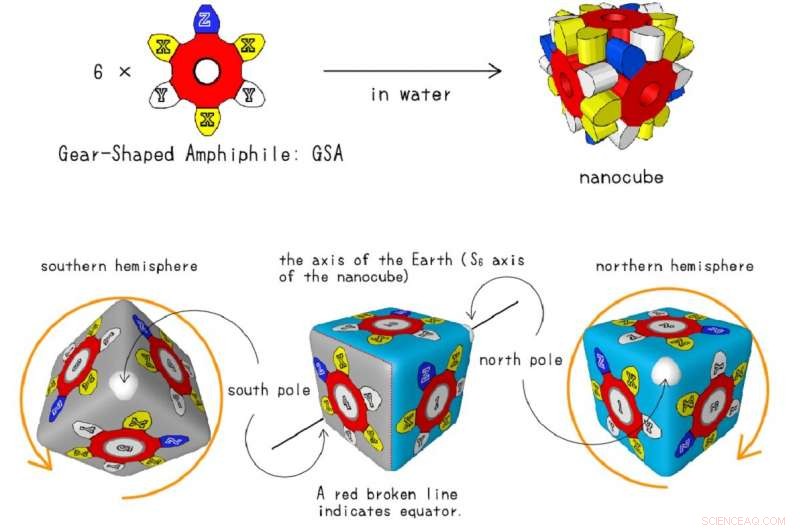
Le nanocube entièrement assemblé est représenté dans cette illustration. Chaque X jaune est un endroit où les chercheurs de l'Université de Tokyo ont utilisé différents atomes sélectionnés pour leur polarisabilité. L'effet combiné de 18 atomes de polarité variable dans chaque nanocube a permis aux chercheurs de mesurer les différences dans la force de dispersion. Crédit :Shuichi Hiraoka, CC-BY.
La force de dispersion est calculée mathématiquement après avoir utilisé une technique appelée calorimétrie de titrage isotherme pour mesurer la quantité de chaleur libérée lorsque les molécules se lient.
Des atomes plus polarisables ont créé des forces de dispersion plus fortes et ont rendu les nanocubes plus stables. En fonction de la valeur estimée de l'effet hydrophobe, la force de dispersion contribue 0,6 à 2,2 fois plus de force d'attraction et de stabilité au cube que l'effet hydrophobe.
Les chercheurs prévoient d'utiliser ces connaissances sur des atomes plus polarisables créant des forces de dispersion plus fortes pour concevoir de futures structures moléculaires artificielles avec des formes plus complexes et des fonctions accrues.
"Par exemple, nous pourrions concevoir des molécules avec des surfaces de liaison plus grandes et placer des atomes polaires le long des bords pour améliorer la stabilité globale grâce à l'attraction des forces de dispersion, " dit Hiraoka.
Résoudre un mystère dans la conception de médicaments
Hiraoka déclare que les mesures pour les nanocubes construits avec de l'hydrogène normal par rapport au deutérium, l'isotope "lourd" de l'hydrogène, devrait être pertinent pour la théorie de la conception de médicaments. Les recherches menées par d'autres groupes avaient conduit à des rapports contradictoires entre les chimistes sur le fait de savoir si l'échange d'hydrogène avec le deutérium deux fois plus lourd et plus gros créerait une force de dispersion plus forte.
En règle générale, les atomes plus gros sont plus polarisables et les chercheurs disposaient de nouvelles données indiquant qu'une polarisabilité accrue conduisait à des forces de dispersion plus fortes. Cependant, dans certains cas, l'hydrogène plus petit produit en fait une force de dispersion plus forte que le deutérium lourd, mais d'autres rapports ont montré la différence opposée ou négligeable entre les deux atomes.
« Dans nos expériences, la différence entropie-enthalpie est complètement équilibrée. L'énergie libre libérée par les nanocubes avec de l'hydrogène ou du deutérium est essentiellement identique, il peut donc n'y avoir aucune différence entre eux, " dit Hiraoka.
Une différence essentielle entre les recherches précédentes et ces expériences est que l'équipe UTokyo a utilisé une condition plus réaliste d'être en solution avec de l'eau et a amplifié l'effet en utilisant la conception nanocube.