
Déplacer un robot, c'est comme manipuler une molécule. Crédit :Willyam Bradberry/Shutterstock.com
Pour nous les humains, un cerveau sain gère tous les détails infimes des mouvements corporels sans exiger une attention consciente. Ce n'est pas le cas pour les robots sans cervelle - en fait, le calcul du mouvement robotique est son propre sous-domaine scientifique.
Mes collègues ici à l'Institute for Protein Design de l'Université de Washington ont découvert comment appliquer un algorithme conçu à l'origine pour aider les robots à passer à un problème totalement différent :la découverte de médicaments. L'algorithme a permis de débloquer une classe de molécules appelées macrocycles peptidiques, qui ont des propriétés pharmaceutiques intéressantes.
Un petit pas, un pas de géant
Les roboticiens qui programment le mouvement le conçoivent dans ce qu'ils appellent des « degrés de liberté ». Prends un bras en métal, par exemple. Le coude, le poignet et les articulations sont mobiles et contiennent donc des degrés de liberté. L'avant-bras, le haut du bras et les sections individuelles de chaque doigt ne le font pas. Si vous souhaitez programmer un androïde pour tendre la main et saisir un objet ou faire un pas calculé, vous devez savoir quels sont ses degrés de liberté et comment les manipuler.
Plus un membre a de degrés de liberté, plus ses mouvements potentiels sont complexes. Les calculs nécessaires pour diriger même des membres robotiques simples sont étonnamment abscons; Ferdinand Freudenstein, un père des champs, une fois appelé les calculs sous-jacents au mouvement d'un membre à sept articulations "le mont Everest de la cinématique".
Freudenstein a développé ses équations cinématiques à l'aube de l'ère informatique dans les années 1950. Depuis, les roboticiens se sont de plus en plus appuyés sur des algorithmes pour résoudre ces énigmes cinématiques complexes. Un algorithme en particulier - connu sous le nom de "fermeture cinématique généralisée" - a battu le problème des sept articulations, permettant aux roboticiens de programmer un contrôle précis dans des mains mécaniques.
Les biologistes moléculaires en ont pris note.
De nombreuses molécules à l'intérieur des cellules vivantes peuvent être conçues comme des chaînes avec des points de pivot, ou degrés de liberté, semblable à de minuscules bras robotiques. Ces molécules fléchissent et se tordent selon les lois de la chimie. Peptides et leurs cousins allongés, protéines, doivent souvent adopter des formes tridimensionnelles précises pour fonctionner. Prédire avec précision les formes complexes des peptides et des protéines permet aux scientifiques comme moi de comprendre leur fonctionnement.
Maîtriser les macrocycles
Alors que la plupart des peptides forment des chaînes droites, un sous-ensemble, connu sous le nom de macrocycles, former des anneaux. Cette forme offre des avantages pharmacologiques distincts. Les structures annulaires sont moins flexibles que les chaînes souples, rendant les macrocycles extrêmement stables. Et parce qu'ils manquent de fins libres, certains peuvent résister à une dégradation rapide dans le corps - un destin par ailleurs courant pour les peptides ingérés.
Les macrocycles naturels tels que la cyclosporine sont parmi les thérapies les plus puissantes identifiées à ce jour. Ils combinent les avantages de stabilité des médicaments à petites molécules, comme l'aspirine, et la spécificité des grands anticorps thérapeutiques, comme l'herceptine. Les experts de l'industrie pharmaceutique considèrent cette catégorie de composés médicinaux comme « attrayante, bien que sous-estimé."
« Il existe une grande diversité de macrocycles dans la nature – dans les bactéries, les plantes, certains mammifères, " dit Gaurav Bhardwaj, auteur principal du nouveau rapport en Science , "et la nature les a développés pour leurs propres fonctions particulières." En effet, de nombreux macrocycles naturels sont des toxines. Cyclosporine, par exemple, affiche une activité antifongique mais agit également comme un puissant immunosuppresseur en clinique, ce qui le rend utile comme traitement de la polyarthrite rhumatoïde ou pour prévenir le rejet d'organes transplantés.
Une stratégie populaire pour produire de nouveaux médicaments macrocycliques consiste à greffer des caractéristiques utiles en médecine sur des squelettes macrocycliques naturels par ailleurs sûrs et stables. "Quand ça marche, ça marche vraiment bien, mais il existe un nombre limité de structures bien caractérisées que nous pouvons utiliser en toute confiance, " dit Bhardwaj. En d'autres termes, les concepteurs de médicaments n'ont eu accès qu'à une poignée de points de départ lors de la fabrication de nouveaux médicaments macrocycliques.
Pour créer des points de départ fiables supplémentaires, son équipe a utilisé la fermeture cinématique généralisée - l'algorithme d'articulation robotique - pour explorer les conformations possibles, ou des formes, que les macrocycles peuvent adopter.
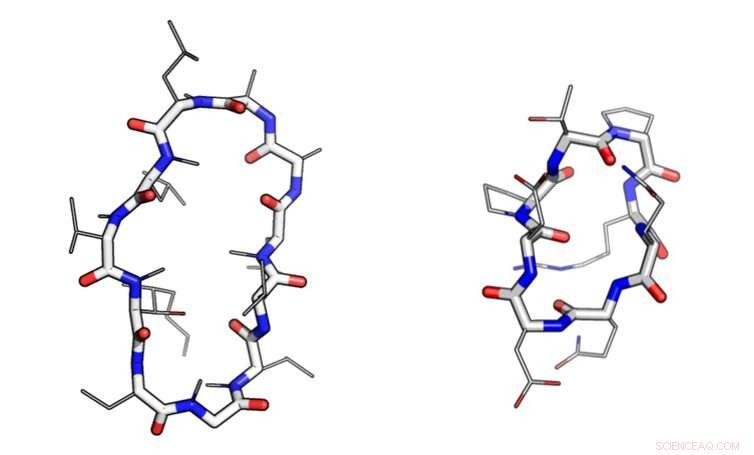
Les macrocycles ont une « chaîne principale » circulaire (indiquée par des lignes épaisses) et de nombreuses « chaînes latérales » (indiquées par des lignes fines). Le macrocycle de gauche - la cyclosporine - a évolué dans un champignon. Celui de droite a été conçu sur ordinateur. Crédit :Ian Haydon/Institute for Protein Design
Algorithmes adaptables
Comme pour les clés, la forme exacte d'un macrocycle est importante. Construisez-en un avec la bonne conformation et vous pourrez débloquer un nouveau remède.
La modélisation de conformations réalistes est "l'une des parties les plus difficiles" de la conception de macrocycles, selon Vikram Mulligan, autre auteur principal du rapport. Mais grâce à l'efficacité de l'algorithme inspiré de la robotique, l'équipe a pu réaliser un « échantillonnage presque exhaustif » de conformations plausibles à « un coût de calcul relativement faible ».
Les calculs étaient si efficaces, En réalité, que la plupart des travaux ne nécessitaient pas de supercalculateur, comme c'est généralement le cas dans le domaine de l'ingénierie moléculaire. Au lieu, des milliers de smartphones appartenant à des volontaires ont été mis en réseau pour former une grille de calcul distribuée, et les calculs scientifiques ont été distribués en morceaux gérables.
Une fois le calcul initial du numéro de smartphone terminé, l'équipe s'est penchée sur les résultats - une collection de centaines de macrocycles jamais vus auparavant. Lorsqu'une douzaine de ces composés ont été synthétisés chimiquement en laboratoire, neuf ont effectivement adopté la conformation prédite. En d'autres termes, les smartphones rendaient avec précision des molécules que les scientifiques peuvent désormais optimiser pour leur potentiel en tant que médicaments ciblés.
L'équipe estime que le nombre de macrocycles pouvant être utilisés en toute confiance comme points de départ pour la conception de médicaments est passé de moins de 10 à plus de 200, grâce à ce travail. Bon nombre des macrocycles nouvellement conçus contiennent des caractéristiques chimiques qui n'ont jamais été vues en biologie.
À ce jour, les médicaments peptidiques macrocycliques se sont révélés prometteurs dans la lutte contre le cancer, maladie cardiovasculaire, inflammation et infection. Grâce aux mathématiques de la robotique, quelques smartphones et une réflexion transversale, les patients pourraient bientôt voir encore plus d'avantages de cette classe prometteuse de molécules.
Cet article a été initialement publié sur The Conversation. Lire l'article original. 