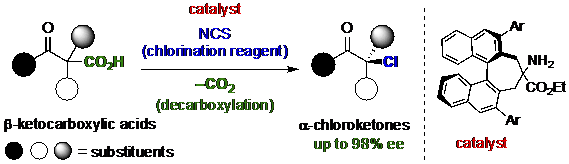
La chloration décarboxylative des acides -céto carboxyliques. Crédit :(c) Université de technologie de Toyohashi
Des chercheurs de l'Université de technologie de Toyohashi dirigés par le professeur agrégé Shibatomi ont développé une nouvelle réaction catalytique pour produire des molécules organiques contenant du chlore sous une forme isomériquement pure (gauche ou droite)
Les molécules n'ont pas de mains, mais certains d'entre eux sont gauchers ou droitiers. De nombreux composés chimiques présentent une caractéristique appelée chiralité, où deux versions, appelées énantiomères, existent pour la même molécule. Bien que leurs atomes soient connectés exactement dans le même ordre, les deux énantiomères sont des images miroir distinctes, comme une paire de mains.
Les énantiomères peuvent avoir des propriétés très différentes. Par exemple, seule la forme droite du glucose vous donne de l'énergie - l'isomère gauche ne peut pas être métabolisé, même s'il a le même goût. De nombreux produits pharmaceutiques sont également chiraux, et souvent un seul énantiomère a un usage médicinal. Par conséquent, les chimistes travaillant sur des molécules complexes ont développé une variété d'astuces pour garantir la pureté des isomères. Cependant, pour certaines réactions, cela reste un défi.
Maintenant, l'équipe de recherche a développé une réaction pour produire une classe importante de composés sous forme pure pour gauchers ou droitiers. Les organohalogénures sont des molécules dans lesquelles un halogène, comme le chlore, est lié au carbone. Beaucoup se trouvent dans la nature, ou utilisé en médecine. Ils peuvent être produits à partir d'une autre famille de composés, acides carboxyliques, en remplaçant simplement un acide par un halogène. Malheureusement, si le composé cible est chiral, cette substitution produit des isomères gauchers et droitiers en quantités égales.
L'équipe de recherche de l'Université de technologie de Toyohashi a résolu ce problème en catalysant la réaction avec un catalyseur lui-même chiral. De nos jours, les catalyseurs se présentent sous une large gamme de formes et de tailles, rivalisant souvent avec la complexité de la molécule cible réelle. « Nous avons passé au crible un large éventail de catalyseurs chiraux, comme l'acide de Lewis, Acide de Brønsted, et catalyseurs à base de Lewis, ", a déclaré l'auteur principal de l'étude, Kazutaka Shibatomi. "Enfin, nous avons trouvé une amine qui nous a donné des organohalogénures avec une pureté énantiomérique allant jusqu'à 98% - même si notre matériau de départ était un mélange 50/50."
Les produits chlorés, connu sous le nom de chlorocétones, sont des éléments constitutifs de molécules chirales plus importantes comme les produits pharmaceutiques. Parce que le chlore n'est que faiblement lié au carbone, il peut être facilement remplacé par un autre atome pour former une nouvelle molécule. En utilisant l'un des nombreux composés produits en pureté énantiomérique par leur nouvelle réaction, l'équipe de recherche a synthétisé la Cathinone, un stimulant naturel.
"La substitution s'effectue de manière simple, façon classique, " dit le professeur associé Shibatomi. " Alors que le chlore laisse la molécule d'un côté, le groupe entrant s'approche du côté opposé. La chiralité du produit ne dépend que de l'arrangement de ces atomes, donc si vous commencez avec un énantiomère pur, vous conservez cette pureté. Cela pourrait ouvrir toute une classe de composés qui étaient auparavant un défi majeur à produire sous forme d'énantiomères purs. »