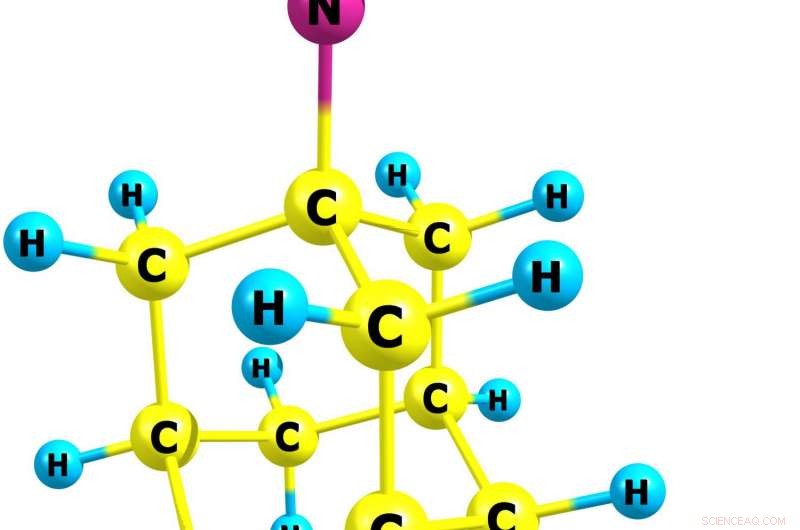
Les chimistes du NIST ont publié les premières données sur les propriétés thermodynamiques du chlorhydrate d'amantadine, utilisé depuis de nombreuses années comme principe actif pharmaceutique de médicaments antiviraux et antiparkinsoniens. Les nouvelles informations peuvent aider à optimiser les conditions de production et de stockage de ce composé important. Sa structure en phase gazeuse a été obtenue par des méthodes de chimie quantique. Dans la structure moléculaire, C est du carbone, H est l'hydrogène, N est l'azote, et Cl est le chlore. Crédit :Bazyleva/NIST
Le chlorhydrate d'amantadine est peut-être le médicament le plus courant dont vous n'avez jamais entendu parler. Ce composé existe depuis des décennies comme base pour les médicaments antiviraux et autres, de la thérapie contre la grippe aux traitements des troubles cérébraux tels que la maladie de Parkinson et la fatigue associée à la sclérose en plaques.
Et encore, ce composé a longtemps été un peu une énigme en raison du manque d'informations sur ses propriétés. Maintenant, des chimistes du National Institute of Standards and Technology (NIST) et des collaborateurs ont publié les toutes premières données sur les propriétés thermodynamiques de cet important produit chimique, y compris des données sur la façon dont il réagit à la chaleur et passe d'un solide à un gaz.
Ces données sont précieuses pour les industries chimiques et pharmaceutiques pour obtenir les rendements de production et la durée de conservation les plus élevés du médicament.
"Nos résultats de recherche ne sont pas directement liés à l'application médicale de ce médicament multifonctionnel, bien que je sois vraiment fasciné par l'étendue de son activité pharmacologique, ", a déclaré Ala Bazyleva, chimiste du NIST.
"Nous avons étudié ses propriétés thermodynamiques et sa décomposition, " dit Bazyleva. " C'est surprenant, étant donné la longue histoire des médicaments à base d'amantadine, qu'il n'y a presque aucune information de ce genre dans la littérature pour beaucoup d'entre eux. Les ingénieurs chimistes doivent souvent s'appuyer sur des estimations et des prédictions basées sur des composés similaires. La collecte de ces informations et le développement de ce type de recommandations sont au cœur de ce que fait notre groupe au NIST."
Le chlorhydrate d'amantadine appartient à la classe des diamantoïdes, une famille de composés dont la structure est basée sur une cage d'atomes de carbone semblable au diamant. L'amantadine a une seule cage de carbone avec un atome d'azote attaché d'un côté. Des études non médicales se sont concentrées sur la forme solide du chlorhydrate d'amantadine, car on s'attendait à ce qu'il se forme de manière désordonnée, ou en plastique, cristaux, comme le font de nombreux diamantoïdes. Il s'avère que, le chlorhydrate d'amantadine ne le fait pas.
Bazyleva a commencé à étudier le chlorhydrate d'amantadine il y a des années alors qu'elle travaillait en Biélorussie sur sa thèse de doctorat, et a poursuivi l'effort au cours de ses études postdoctorales en Allemagne et au Canada. Mais les progrès étaient lents, en partie parce que le chlorhydrate d'adamantine passe d'un solide directement à un gaz (un processus appelé sublimation) et se désagrège simultanément, ou se décompose. Elle avait besoin d'un modèle expliquant ce processus complexe, celui qui intègre détaillé, calculs de haut niveau de la chimie quantique. Elle a finalement eu accès à cette capacité de calcul après avoir commencé à travailler avec le groupe du Centre de recherche sur la thermodynamique (TRC) du NIST à Boulder il y a plusieurs années.
"Le NIST a joué un rôle fondamental dans la facilitation de la composante modélisation, " dit Bazileva. " En particulier, la combinaison unique d'installations, les logiciels et l'expertise en calculs chimiques quantiques nous ont permis d'appliquer des calculs de haut niveau pour avoir un aperçu de la structure et de la stabilité du médicament en phase gazeuse."
Alors que le composé se comporte comme s'il était ionique (composé de pièces chargées positivement et négativement, bien que globalement neutre) sous forme cristalline solide et lorsqu'il est dissous dans un liquide, des calculs de chimie quantique ont révélé qu'il se décompose en deux composés neutres en phase gazeuse.