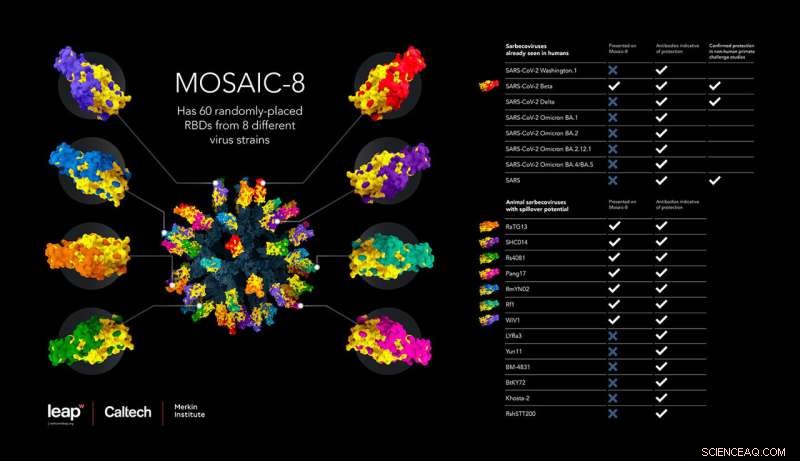
Cette infographie illustre le nouveau vaccin, composé de RBD de huit virus différents. Le tableau montre le large spectre des variantes du SRAS-CoV-2 et des coronavirus apparentés contre lesquels le vaccin induit une protection. Crédit :Wellcome Leap, Caltech, Institut Merkin
Un nouveau type de vaccin offre une protection contre une variété de bêtacoronavirus de type SRAS, y compris les variantes du SRAS-CoV-2, chez les souris et les singes, selon une étude menée par des chercheurs du laboratoire de Pamela Bjorkman de Caltech, professeur de biologie David Baltimore et Bioingénierie.
Les bêtacoronavirus, y compris ceux qui ont causé les pandémies de SRAS, de MERS et de COVID-19, sont un sous-ensemble de coronavirus qui infectent les humains et les animaux. Le vaccin fonctionne en présentant au système immunitaire des morceaux des protéines de pointe du SRAS-CoV-2 et de sept autres bêtacoronavirus de type SRAS, attachés à une structure de nanoparticules protéiques, pour induire la production d'un large spectre d'anticorps à réaction croisée. Notamment, lorsqu'ils ont été vaccinés avec cette nanoparticule dite mosaïque, les modèles animaux ont été protégés contre un coronavirus supplémentaire, le SRAS-CoV, qui n'était pas l'un des huit représentés sur le vaccin à nanoparticules.
"Les animaux vaccinés avec les nanoparticules de la mosaïque 8 ont suscité des anticorps qui reconnaissaient pratiquement toutes les souches de bétacoronavirus de type SRAS que nous avons évaluées", explique le chercheur postdoctoral de Caltech Alexander Cohen (Ph.D. '21), co-premier auteur de la nouvelle étude. "Certains de ces virus pourraient être liés à la souche qui cause la prochaine épidémie de bêtacoronavirus de type SRAS, donc ce que nous voulons vraiment, ce serait quelque chose qui cible cet entre groupe de virus. Nous pensons que nous l'avons."
La recherche apparaît dans un article de la revue Science le 5 juillet.
"Le SRAS-CoV-2 s'est avéré capable de créer de nouvelles variantes qui pourraient prolonger la pandémie mondiale de COVID-19", déclare Bjorkman, qui est également professeur à l'Institut Merkin et directeur général de la biologie et du génie biologique. "En outre, le fait que trois bêtacoronavirus - le SRAS-CoV, le MERS-CoV et le SRAS-CoV-2 - se sont propagés aux humains à partir d'hôtes animaux au cours des 20 dernières années illustre la nécessité de fabriquer des vaccins largement protecteurs."
Une protection aussi large est nécessaire, dit Bjorkman, "car nous ne pouvons pas prédire quel virus parmi le grand nombre d'animaux évoluera à l'avenir pour infecter les humains et provoquer une autre épidémie ou pandémie. Ce que nous essayons de faire, c'est de faire un vaccin tout-en-un protégeant contre les bêtacoronavirus de type SRAS, quels que soient les virus animaux susceptibles d'évoluer pour permettre l'infection et la propagation humaines.Ce type de vaccin protégerait également contre les variantes actuelles et futures du SRAS-CoV-2 sans nécessiter de mise à jour. "
Comment ça marche :un vaccin composé de domaines de pointe provenant de huit différents coronavirus de type SRAS
La technologie vaccinale pour attacher des morceaux d'un virus à des nanoparticules de protéines a été initialement développée par des collaborateurs de l'Université d'Oxford. La base de la technologie est une minuscule structure en forme de cage (une "nanoparticule") composée de protéines conçues pour avoir des appendices "collants" à sa surface, sur lesquels les chercheurs peuvent attacher des protéines virales étiquetées. Ces nanoparticules peuvent être préparées pour présenter des morceaux d'un seul virus (nanoparticules "homotypiques") ou des morceaux de plusieurs virus différents (nanoparticules "mosaïques"). Lorsqu'il est injecté à un animal, le vaccin à nanoparticules présente ces fragments viraux au système immunitaire. Cela induit la production d'anticorps, des protéines du système immunitaire qui reconnaissent et combattent des agents pathogènes spécifiques, ainsi que des réponses immunitaires cellulaires impliquant les lymphocytes T et les cellules immunitaires innées.
Dans cette étude, les chercheurs ont choisi huit bêtacoronavirus différents de type SRAS – dont le SRAS-CoV-2, le virus qui a causé la pandémie de COVID-19, ainsi que sept virus animaux apparentés qui pourraient avoir le potentiel de déclencher une pandémie chez l’homme – et fragments attachés de ces huit virus sur l'échafaudage de nanoparticules. L'équipe a choisi des fragments spécifiques des structures virales, appelés domaines de liaison aux récepteurs (RBD), qui sont essentiels pour que les coronavirus pénètrent dans les cellules humaines. En fait, les anticorps humains qui neutralisent les coronavirus ciblent principalement les RBD du virus.
L'idée est qu'un tel vaccin pourrait inciter le corps à produire des anticorps qui reconnaissent largement les bêtacoronavirus de type SRAS pour combattre les variants en plus de ceux présentés sur la nanoparticule en ciblant les caractéristiques communes des RBD viraux. Cette conception vient de l'idée que la diversité et l'arrangement physique des RBD sur la nanoparticule concentreront la réponse immunitaire vers des parties du RBD qui sont partagées par toute la famille des coronavirus du SRAS, obtenant ainsi une immunité pour tous. Les données rapportées dans Science démontre aujourd'hui l'efficacité potentielle de cette approche.
Concevoir des expériences pour mesurer la protection du vaccin chez la souris
Le vaccin résultant (ici surnommé mosaïque-8) est composé de RBD de huit coronavirus. Des expériences précédentes menées par le laboratoire Bjorkman ont montré que la mosaïque-8 incite les souris à produire des anticorps qui réagissent à une variété de coronavirus dans une boîte de laboratoire. Dirigée par Cohen, la nouvelle étude visait à s'appuyer sur cette recherche pour voir si la vaccination avec le vaccin mosaïque-8 pouvait induire des anticorps protecteurs chez un animal vivant lors d'une provocation (en d'autres termes, une infection) par le SRAS-CoV-2 ou le SRAS-CoV .
L'équipe visait à comparer le degré de protection contre l'infection fourni par une nanoparticule recouverte de différents fragments de coronavirus (mosaïque-8) par rapport à une nanoparticule recouverte uniquement de fragments de SARS-CoV-2 (une nanoparticule "homotypique").
L'équipe a mené trois séries d'expériences sur des souris. Dans l'un, le contrôle, ils ont inoculé à des souris uniquement la structure nue de la cage de nanoparticules sans aucun fragment de virus attaché. Un deuxième groupe de souris a reçu une injection d'une nanoparticule homotypique recouverte uniquement de RBD du SRAS-CoV-2, et un troisième groupe a reçu une injection de nanoparticules mosaïque-8. Un objectif expérimental était de voir si l'inoculation de mosaïque-8 protégerait les animaux contre le SRAS-CoV-2 au même degré que les animaux homotypiques immunisés contre le SRAS-CoV-2 ; un deuxième objectif était d'évaluer la protection contre un soi-disant "virus incompatible" - un virus qui n'était pas représenté par un RBD sur la nanoparticule mosaïque-8.
Notamment, les huit souches de coronavirus recouvrant la nanoparticule de mosaïque n'incluaient pas intentionnellement le SRAS-CoV, le virus qui a provoqué la pandémie de SRAS initiale au début des années 2000. Ainsi, l'équipe visait également à étudier le degré de protection contre une provocation avec le virus SRAS-CoV d'origine, en l'utilisant pour représenter un bêtacoronavirus inconnu de type SRAS qui pourrait se répandre chez l'homme.
Les souris utilisées dans les expériences ont été génétiquement modifiées pour exprimer le récepteur ACE2 humain, qui est le récepteur des cellules humaines utilisé par le SRAS-CoV-2 et les virus apparentés pour pénétrer dans les cellules pendant l'infection. Dans ce modèle de provocation animale, des souris non vaccinées meurent si elles sont infectées par un bêtacoronavirus de type SRAS, fournissant ainsi un test rigoureux pour évaluer le potentiel de protection contre les infections et les maladies chez l'homme.
Le vaccin Mosaic protège les souris contre un bêtacoronavirus semblable à celui du SRAS
Comme prévu, les souris inoculées avec la structure nue des nanoparticules sont mortes lorsqu'elles ont été infectées par le SRAS-CoV ou le SRAS-CoV-2. Les souris qui ont été inoculées avec une nanoparticule homotypique uniquement recouverte de RBD du SRAS-CoV-2 ont été protégées contre l'infection par le SRAS-CoV-2 mais sont décédées après exposition au SRAS-CoV. Ces résultats suggèrent que les vaccins candidats homotypiques actuels à base de nanoparticules contre le SRAS-CoV-2 en cours de développement ailleurs seraient efficaces contre le SRAS-CoV-2, mais pourraient ne pas protéger largement contre d'autres bétacoronavirus de type SRAS traversant des réservoirs animaux ou contre le futur SRAS-CoV-2 variantes.
Cependant, toutes les souris inoculées avec des nanoparticules de mosaïque-8 ont survécu aux défis du SRAS-CoV-2 et du SRAS-CoV sans perte de poids ni autres pathologies importantes.
La recherche sur les primates non humains confirme également l'efficacité du vaccin mosaïque
L'équipe a ensuite réalisé des expériences de provocation similaires chez des primates non humains, cette fois en utilisant le candidat vaccin le plus prometteur, la mosaïque-8, et en comparant les effets de la vaccination par la mosaïque-8 par rapport à l'absence de vaccination dans les études de provocation animale. Lorsqu'ils ont été inoculés avec de la mosaïque-8, les animaux ont montré peu ou pas d'infection détectable lorsqu'ils ont été exposés au SRAS-CoV-2 ou au SRAS-CoV, démontrant à nouveau le potentiel du vaccin candidat mosaïque-8 à protéger les variantes actuelles et futures du virus à l'origine de la pandémie de COVID-19 ainsi que contre les futures propagations virales potentielles de bêtacoronavirus de type SRAS provenant d'hôtes animaux.
Fait important, en collaboration avec le virologue Jesse Bloom (Ph.D. '07) du Fred Hutchinson Cancer Research Center, l'équipe a découvert que les anticorps provoqués par la mosaïque-8 ciblaient les éléments les plus courants des RBD dans un ensemble diversifié d'autres SRAS- comme les bétacoronavirus - la partie dite «conservée» du RBD - fournissant ainsi des preuves du mécanisme hypothétique par lequel le vaccin serait efficace contre de nouvelles variantes du SRAS-CoV-2 ou des bétacoronavirus animaux de type SRAS. En revanche, les injections de nanoparticules homotypiques du SRAS-CoV-2 ont suscité des anticorps contre des régions RBD principalement spécifiques à la souche, ce qui suggère que ces types de vaccins protégeraient probablement contre le SRAS-CoV-2 mais pas contre les nouvelles variantes ou les virus animaux émergents potentiels.
Dans une prochaine étape, Bjorkman et ses collègues évalueront les immunisations aux nanoparticules de mosaïque-8 chez l'homme dans le cadre d'un essai clinique de phase 1 soutenu par la Coalition for Epidemic Preparedness Initiative (CEPI). Pour se préparer à l'essai clinique, qui recrutera en grande partie des personnes qui ont été vaccinées et/ou précédemment infectées par le SRAS-CoV-2, le laboratoire Bjorkman prévoit des expériences précliniques sur des modèles animaux pour comparer les réponses immunitaires chez des animaux précédemment vaccinés avec un COVID-19 actuel. 19 vaccin aux réponses chez les animaux qui sont immunologiquement naïfs en ce qui concerne l'infection ou la vaccination par le SRAS-CoV-2.
« Nous avons parlé du besoin de diversité dans le développement de vaccins depuis le tout début de la pandémie », déclare le Dr Richard J. Hatchett, PDG du CEPI. « La percée présentée dans l'étude du laboratoire Bjorkman démontre un énorme potentiel pour une stratégie qui poursuit une nouvelle plate-forme vaccinale dans son ensemble, surmontant potentiellement les obstacles créés par de nouvelles variantes. Je suis ravi d'annoncer que le CEPI soutiendra cette nouvelle approche de la prévention des pandémies en phase I essais cliniques. La vitesse accélérée atteinte par l'étude après avoir reçu le financement de Wellcome Leap a facilité notre relation avec eux aujourd'hui. Les données sur les primates non humains sont extrêmement encourageantes et nous sommes ravis de soutenir la prochaine phase des essais. La technologie d'immunisation aux nanoparticules pourrait protéger contre de nombreuses souches de coronavirus