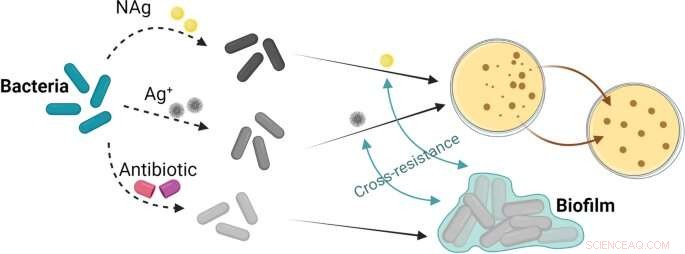
Résumé graphique. Crédit :DOI :10.1186/s12951-021-01027-8
De nouvelles recherches de l'Université de technologie de Sydney (UTS) ont révélé que les agents pathogènes qui forment des biofilms peuvent évoluer pour survivre au traitement au nanoargent. L'étude est la première à démontrer qu'un traitement à long terme au nanoargent peut augmenter le risque d'infections récurrentes.
La recherche est publiée dans le Journal de nanobiotechnologie .
Le nanoargent est un puissant antimicrobien qui est actuellement utilisé dans les dispositifs médicaux tels que les cathéters internes, ainsi que des pansements, en particulier pour les brûlures, pour combattre ou prévenir les infections. C'est également l'une des nanoparticules antimicrobiennes les plus commercialisées, et a été incorporé dans des produits de consommation à partir de produits de soins personnels, tels que les savons et les dentifrices, aux machines à laver et aux réfrigérateurs, même des produits pour enfants, comme dans les chaussettes pour enfants pour éviter les odeurs.
Des chercheurs de l'institut iThree de l'UTS ont étudié les phénomènes d'adaptation du nanoargent chez la bactérie Pseudomonas aeruginosa, sous sa forme de biofilm de croissance, et a observé un nouveau mécanisme d'adaptation non vu dans les études précédentes sur la croissance planctonique. Après un traitement prolongé, nanosilver a tué 99,99% de la population bactérienne avec seulement 0,01% des cellules survivant plus longtemps. Cette infime fraction de « persistants » a repris une croissance normale à l'arrêt du traitement aux nanoparticules.
« Comprendre comment les agents pathogènes développent des mécanismes d'adaptation aux nanoparticules est essentiel dans nos efforts pour surmonter les phénomènes, y compris dans les biofilms en tant que principale forme de croissance des bactéries pathogènes. Il s'agit de protéger l'efficacité d'antimicrobiens alternatifs importants, comme le nanoargent, en cette ère de résistance croissante aux antibiotiques, ", a déclaré l'auteur principal, le Dr Cindy Gunawan.
Le premier auteur de l'étude, Dr Riti Mann, a déclaré que les résultats de la recherche aideront également à développer des stratégies pour une meilleure gestion de l'utilisation des nanoparticules comme antimicrobiens, en particulier ceux impliquant des expositions à long terme.
« Sur la base de cette étude, nous recommandons de surveiller les patients non seulement pendant, mais aussi après une utilisation prolongée d'un traitement aux nanoparticules pour se prémunir contre les infections récurrentes.
« La preuve scientifique que les bactéries peuvent s'adapter aux nanoparticules signifie que nous avons besoin d'une réglementation efficace de l'utilisation des nanoparticules, avec une évaluation claire des risques par rapport aux avantages et des cibles antimicrobiennes claires. Avec le développement limité de nouveaux antibiotiques efficaces au cours des dernières décennies, nous devons préserver l'efficacité des antimicrobiens alternatifs pour lutter contre les infections incurables, sauver des vies et des milliards de dollars en soins de santé, " a déclaré le Dr Gunawan.
La bactérie utilisée dans l'étude, Pseudomonas aeruginosa, se fixent souvent sur les surfaces du cathéter, ainsi qu'aux plaies et aux muqueuses pulmonaires, faire pousser des biofilms, qui peut être difficile à contrôler.