Nano Lett. 2021, 21, 8, 3596-3603
Le nouveau test de flux latéral Vigilant est moins cher, plus facile à utiliser et aussi fiable que le test PCR de référence actuel pour le diagnostic de l'infection par le SRAS-CoV-2.
Un test de flux latéral SARS-CoV-2 qui combine deux enzymes bactériennes avec des séquences génétiques et quelques sondes est moins cher et plus facile à utiliser que les tests PCR tout en produisant des résultats d'une fiabilité comparable. Appelé Vigilant et conçu chez KAUST, le test peut détecter de très petites quantités d'ARN viral dans un échantillon.
"Plusieurs types de tests de flux latéral sont actuellement disponibles ou en cours de recherche pour détecter le SARS-CoV-2, ", déclare Tin Marsic, étudiant au doctorat de la KAUST. "Selon la façon dont ils travaillent, ils ont tous des inconvénients, y compris la détection du virus seulement plusieurs jours après l'infection ou la production de résultats faussement positifs et faussement négatifs." Tests PCR, qui se déroulent en laboratoire, produisent des résultats plus fiables mais sont coûteux et nécessitent un équipement sophistiqué et un personnel qualifié.
« Vigilant peut être effectué dans des environnements non-laboratoires et est nettement moins cher et plus facile à utiliser que les tests PCR, " dit Marsic.
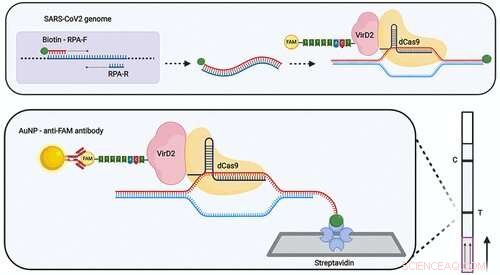
La première étape critique de la plateforme Vigilant implique une technique appelée amplification par transcription inverse-recombinase polymérase (RT-RPA) pour faire de nombreuses copies d'une région spécifique sur le génome du SARS-CoV-2, s'il existe dans l'échantillon d'écouvillonnage du nez et de la gorge d'une personne. Les tests PCR amplifient également les séquences de gènes viraux dans les échantillons, mais impliquent de soumettre les échantillons à plusieurs cycles à haute et basse température. La RT-RPA peut être effectuée à température ambiante avec un équipement beaucoup moins cher et facile à utiliser.
Tous les gènes amplifiés par le SRAS-CoV-2 dans le produit de ce processus sont marqués avec une molécule appelée biotine, puis ajouté à un tube à essai contenant le complexe de détection spécialement conçu par KAUST.
Ce complexe est formé de deux enzymes. D'un côté, une enzyme bactérienne appelée Cas9 est conjuguée à un guide ARN qui ne reconnaît et ne s'attache qu'à la séquence du gène SARS-CoV-2 correspondante. De l'autre côté, une autre enzyme bactérienne appelée VirD2 est attachée à une séquence nucléotidique marquée par fluorescence.
Les gouttes de la réaction entre le complexe et le produit RT-RPA sont ensuite ajoutées à une bandelette réactive à flux latéral imprégnée d'une protéine reconnaissant la biotine appelée streptavidine à une extrémité et d'un anticorps fluorescent reconnaissant la sonde de l'autre. Si l'échantillon contient des séquences de gènes SARS-CoV-2, ils se seront liés au complexe VirD2-Cas9. Un résultat positif se produit lorsque deux lignes visibles apparaissent. La première ligne est l'endroit où la biotine sur l'amplicon SARS-CoV-2 se lie à la streptavidine. La deuxième ligne est l'endroit où l'étiquette fluorescente à l'autre extrémité du complexe se fixe à l'anticorps de la bandelette. Un résultat négatif ne se présente que sous la forme d'une seule ligne causée par la liaison fluorescente de l'étiquette à l'anticorps.
« Nous travaillons désormais à rendre notre plateforme Vigilant plus conviviale en la couplant à une technique d'amplification encore plus simple, " dit Magdy Mahfouz, bio-ingénieure de KAUST, qui a dirigé la recherche. « Nous travaillons également à la production d'autres tests de diagnostic efficaces et rapides qui peuvent détecter les acides nucléiques pour permettre des tests sur le lieu de soins pour les agents pathogènes, y compris les virus et les marqueurs de la maladie."