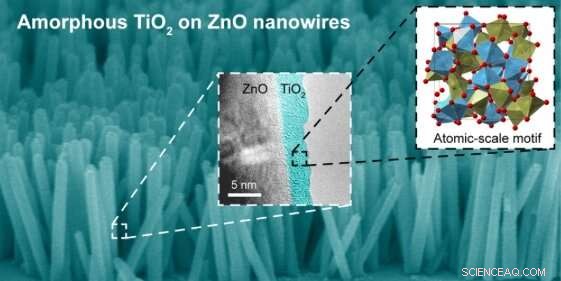
(Contexte) Une image au microscope électronique à balayage en fausses couleurs de nanofils d'oxyde de zinc (ZnO) recouverts de dioxyde de titane, ou de l'oxyde de titane (TiO2). En moyenne, les nanofils sont 10 fois plus longs que larges. L'encart en pointillés blancs contient une image au microscope électronique à transmission haute résolution qui fait la distinction entre le noyau de ZnO et l'enveloppe d'oxyde de titane. L'encart en pointillés noirs présente un modèle structurel de la coquille de titane amorphe, avec les cercles rouges correspondant aux atomes d'oxygène et les polyèdres vert et bleu correspondant aux atomes de titane sous-coordonnés et coordonnés, respectivement. Crédit :Laboratoire national de Brookhaven
L'énergie solaire récoltée par les semi-conducteurs, des matériaux dont la résistance électrique se situe entre celle des métaux ordinaires et des isolants, peut déclencher des réactions électrochimiques de surface pour générer des carburants propres et durables tels que l'hydrogène. Des catalyseurs hautement stables et actifs sont nécessaires pour accélérer ces réactions, en particulier pour diviser les molécules d'eau en oxygène et en hydrogène. Les scientifiques ont identifié plusieurs semi-conducteurs puissants absorbant la lumière comme catalyseurs potentiels; cependant, à cause de la photocorrosion, beaucoup de ces catalyseurs perdent leur activité pour la réaction de séparation de l'eau. Corrosion induite par la lumière, ou photocorrosion, se produit lorsque le catalyseur lui-même subit des réactions chimiques (oxydation ou réduction) via des porteurs de charge (électrons et "trous, " ou électrons manquants) générés par l'excitation lumineuse. Cette dégradation limite l'activité catalytique.
Maintenant, des scientifiques du Center for Functional Nanomaterials (CFN) - une installation d'utilisateurs du département américain de l'énergie (DOE) du bureau des sciences du laboratoire national de Brookhaven - ont mis au point une technique pour optimiser l'activité d'un tel catalyseur :de 500 nanomètres de long mais nanostructures filaires relativement fines (40 à 50 nanomètres), ou des nanofils, en oxyde de zinc (ZnO). Leur technique, décrite dans un article publié en ligne dans Lettres nano le 3 mai - consiste à traiter chimiquement la surface des nanofils de manière à ce qu'ils puissent être uniformément recouverts d'un film ultrafin (deux à trois nanomètres d'épaisseur) de dioxyde de titane (oxyde de titane), qui agit à la fois comme catalyseur et couche protectrice.
La recherche dirigée par le CFN est une collaboration entre la National Synchrotron Light Source II (NSLS-II) de Brookhaven Lab - une autre installation utilisateur du DOE Office of Science - et Computational Science Initiative (CSI); le Center for Computational Materials Science du Naval Research Laboratory; et le Département de science des matériaux et de génie chimique de l'Université Stony Brook.

(Assis de face) Iradwikanari Waluyo, Mingzhao Liu, Dario Stacchiola, (debout de face) Mehmet Topsakal, Mark Hybertsen, Deyu Lu, et Eli Stavitski à la ligne de lumière de spectroscopie de coque intérieure de la source nationale de lumière synchrotron II (NSLS-II) de Brookhaven Lab. Les scientifiques ont effectué des expériences de spectroscopie d'absorption des rayons X au NSLS-II pour caractériser l'état chimique des revêtements de dioxyde de titane (oxyde de titane) sur des nanofils d'oxyde de zinc. Ils ont traité chimiquement les nanofils pour fabriquer les revêtements, qui augmentent l'efficacité des nanofils dans la catalyse de la réaction de séparation de l'eau qui produit de l'oxygène et de l'hydrogène, un carburant durable, plus susceptible d'adhérer. Ces résultats de caractérisation ont été couplés à l'imagerie par microscopie électronique et à des analyses théoriques pour générer un modèle de la structure atomique amorphe (non cristalline) de l'oxyde de titane. Crédit :Laboratoire national de Brookhaven
"Les nanofils sont des structures catalytiques idéales car ils ont une grande surface pour absorber la lumière, et le ZnO est un matériau abondant sur terre qui absorbe fortement la lumière ultraviolette et a une mobilité électronique élevée, " a déclaré Mingzhao Liu, auteur co-correspondant et responsable de l'étude, un scientifique du groupe de science et de catalyse de l'interface du CFN. "Toutefois, par eux-mêmes, Les nanofils de ZnO n'ont pas une activité catalytique ou une stabilité suffisamment élevée pour la réaction de séparation de l'eau. En les enduisant uniformément de films ultrafins d'oxyde de titane, un autre matériau à faible coût qui est chimiquement plus stable et plus actif pour favoriser le transfert de charge interfacial, améliore ces propriétés pour augmenter l'efficacité de la réaction de 20 % par rapport aux nanofils de ZnO pur. »
Pour "mouiller" la surface des nanofils pour le revêtement en oxyde de titane, les scientifiques ont combiné deux méthodes de traitement de surface :le recuit thermique et la pulvérisation au plasma à basse pression. Pour le recuit thermique, ils ont chauffé les nanofils dans un environnement d'oxygène pour éliminer les défauts et les contaminants; pour la pulvérisation au plasma, ils ont bombardé les nanofils avec des ions oxygène gazeux énergétiques (plasma), qui a éjecté des atomes d'oxygène de la surface de ZnO.
"Ces traitements modifient la chimie de surface des nanofils de telle sorte que le revêtement d'oxyde de titane est plus susceptible d'adhérer lors du dépôt de la couche atomique, " expliqua Liu. " Dans le dépôt de couche atomique, différents précurseurs chimiques réagissent avec une surface de matériau de manière séquentielle pour construire des films minces avec une couche d'atomes à la fois."
Les scientifiques ont imagé les structures de la coque des nanofils avec des microscopes électroniques à transmission au CFN, projeter un faisceau d'électrons à travers l'échantillon et détecter les électrons transmis. Cependant, parce que la couche d'oxyde de titane ultrafine n'est pas cristalline, ils avaient besoin d'utiliser d'autres méthodes pour déchiffrer sa structure « amorphe ». Ils ont réalisé des expériences de spectroscopie d'absorption des rayons X sur deux lignes de lumière NSLS-II :la spectroscopie de coque interne (ISS) et la spectroscopie de rayons X in situ et Operando (IOS).
"Les énergies des rayons X sur les deux lignes de lumière sont différentes, ainsi les rayons X interagissent avec différents niveaux électroniques dans les atomes de titane, " a déclaré le co-auteur Eli Stavitski, Physicien de la ligne de lumière de l'ISS. "Les spectres d'absorption complémentaires générés par ces expériences ont confirmé la structure hautement amorphe de l'oxyde de titane, avec des domaines cristallins limités à quelques nanomètres. Les résultats nous ont également donné des informations sur l'état de valence (charge) des atomes de titane - combien d'électrons se trouvent dans la couche la plus externe entourant le noyau - et la sphère de coordination, ou le nombre d'atomes d'oxygène voisins les plus proches."
Les théoriciens et les informaticiens de l'équipe ont ensuite déterminé la structure atomique la plus probable associée à ces spectres expérimentaux. Dans les matériaux à structure cristalline, l'arrangement d'un atome et de ses voisins est le même dans tout le cristal. Mais les structures amorphes manquent de cette uniformité ou de cet ordre à longue distance.
"Nous devions trouver la bonne combinaison de configurations structurelles responsables de la nature amorphe du matériau, " a expliqué l'auteur co-correspondant Deyu Lu, un scientifique du groupe de théorie et de calcul du CFN. "D'abord, nous avons passé au crible une base de données structurelle existante et identifié plus de 300 structures locales pertinentes à l'aide d'outils d'analyse de données précédemment développés par l'ancien postdoctorant du CFN Mehmet Topsakal et le chercheur en informatique du CSI Shinjae Yoo. Nous avons calculé les spectres d'absorption des rayons X pour chacune de ces structures et sélectionné 11 structures représentatives comme fonctions de base pour s'adapter à nos résultats expérimentaux. De cette analyse, nous avons déterminé le pourcentage d'atomes de titane avec une coordination locale particulière."
L'analyse a montré qu'environ la moitié des atomes de titane étaient "sous-coordonnés". En d'autres termes, ces atomes de titane n'étaient entourés que de quatre ou cinq atomes d'oxygène, contrairement aux structures des formes les plus courantes d'oxyde de titane, qui ont six atomes d'oxygène voisins.
Pour valider le résultat théorique, Lu et les autres théoriciens—Mark Hybertsen, chef du groupe Théorie et calcul CFN; CFN postdoctoral Sencer Selcuk; et ancien postdoctorant CFN John Lyons, maintenant un physicien au Naval Research Lab, a créé un modèle à l'échelle atomique de la structure amorphe de l'oxyde de titane. Ils ont appliqué la technique informatique de la dynamique moléculaire pour simuler le processus de recuit qui a produit la structure amorphe. Avec ce modèle, ils ont également calculé le spectre d'absorption des rayons X de l'oxyde de titane; leurs calculs ont confirmé qu'environ 50 pour cent des atomes de titane étaient sous-coordonnés.
"Ces deux méthodes indépendantes nous ont donné un message cohérent sur la structure locale de l'oxyde de titane, " dit Lou.
"Les atomes entièrement coordonnés ne sont pas très actifs car ils ne peuvent pas se lier aux molécules avec lesquelles ils font de la chimie dans les réactions, " explique Stavitski. " Pour rendre les catalyseurs plus actifs, nous devons réduire leur coordination."
"Le comportement de transport de l'oxyde de titane amorphe est très différent de celui de l'oxyde de titane en vrac, " a ajouté Liu. " L'oxyde de titane amorphe peut transporter efficacement à la fois les trous et les électrons en tant que porteurs de charge actifs, qui entraînent la réaction de séparation de l'eau. Mais pour comprendre pourquoi, nous devons connaître les principaux motifs à l'échelle atomique."
Au meilleur de leur connaissance, les scientifiques sont les premiers à étudier l'oxyde de titane amorphe à une échelle aussi fine.
"Pour comprendre l'évolution structurelle de l'oxyde de titane au niveau atomique, nous avions besoin de scientifiques sachant cultiver des matières actives, comment caractériser ces matériaux avec les outils qui existent au CFN et au NSLS-II, et comment donner un sens aux résultats de la caractérisation en tirant parti des outils théoriques, " dit Stavitski.
Prochain, l'équipe étendra son approche consistant à combiner l'analyse des données de spectroscopie expérimentale et théorique aux matériaux pertinents pour la science de l'information quantique (QIS). Le domaine émergent du QIS tire parti des effets quantiques en physique, ou les comportements et interactions étranges qui se produisent à très petite échelle. Ils espèrent que les utilisateurs du CFN et du NSLS-II utiliseront l'approche dans d'autres domaines de recherche, comme le stockage d'énergie.