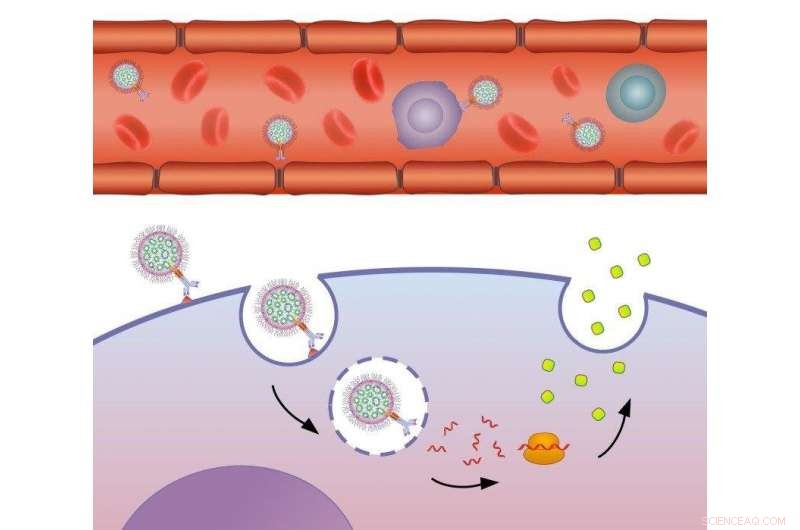
Illustration schématique du mécanisme par lequel les nanoparticules ciblées du laboratoire modulent l'expression des gènes dans la cellule cible. Crédit :Nuphar Veiga/American Friends of Tel Aviv University.
Fournir une charge utile thérapeutique efficace à des cellules cibles spécifiques avec peu d'effets indésirables est considéré par beaucoup comme le Saint Graal de la recherche médicale. Une nouvelle étude de l'Université de Tel Aviv explore une approche biologique pour diriger des nanotransporteurs chargés de protéines « changeurs de jeu » vers des cellules spécifiques. La méthode révolutionnaire peut s'avérer utile dans le traitement d'une myriade de tumeurs malignes, maladies inflammatoires et maladies génétiques rares.
le professeur Dan Peer, directeur du Laboratoire de nanomédecine de précision à l'École de biologie cellulaire moléculaire de la Faculté des sciences de la vie de TAU, a dirigé les recherches pour la nouvelle étude, qui a été menée par l'étudiant diplômé de la TAU Nuphar Veiga et ses collègues de laboratoire Meir Goldsmith, Yasmine Granot, Daniel Rosenblum, Niels Dammes, Ranit Kedmi et Srinivas Ramishetti. La recherche a été publiée dans Communication Nature .
Au cours des dernières années, les transporteurs lipidiques encapsulant des ARN messagers (ARNm) se sont révélés extrêmement utiles pour modifier les expressions protéiques d'une multitude de maladies. Mais diriger ces informations vers des cellules spécifiques est resté un défi majeur.
« Dans notre nouvelle recherche, nous avons utilisé des transporteurs chargés d'ARNm - des nanovéhicules transportant un ensemble d'instructions génétiques via une plate-forme biologique appelée ASSET - pour cibler les instructions génétiques d'une protéine anti-inflammatoire dans les cellules immunitaires, ", explique le professeur Peer. "Nous avons pu démontrer que la protéine anti-inflammatoire sélective dans les cellules cibles entraînait une réduction des symptômes et de la gravité de la maladie dans la colite.
"Cette recherche est révolutionnaire. Elle ouvre la voie à l'introduction d'un ARNm qui pourrait coder n'importe quelle protéine manquante dans les cellules, avec des applications directes pour la génétique, maladies inflammatoires et auto-immunes, sans oublier le cancer, dans lequel certains gènes se surexpriment."
ASSET (Anchored Secondary scFv Enabling Targeting) utilise une approche biologique pour diriger les nanotransporteurs dans des cellules spécifiques afin de favoriser la manipulation des gènes.
"Cette étude ouvre de nouvelles voies dans l'administration cellulaire de molécules d'ARNm et pourrait finalement introduire l'ARNm anti-inflammatoire spécifique (interleukine 10) en tant que nouvelle modalité thérapeutique pour les maladies inflammatoires de l'intestin, " dit Mme Veiga.
« La production ciblée de protéines à base d'ARNm a des applications à la fois thérapeutiques et de recherche, " conclut-elle. " A l'avenir, nous avons l'intention d'utiliser la livraison ciblée d'ARNm pour la recherche de nouvelles thérapies traitant les troubles de l'inflammation, cancer et maladies génétiques rares.