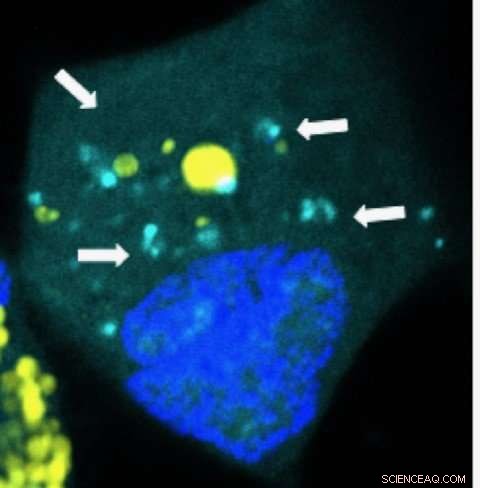
Nanoparticules libérant des microARN (bleu clair) à l'intérieur d'une cellule cancéreuse du cerveau humain. Crédit :Yuan Rui, John Hopkins
Dans une étude de « preuve de concept », Les scientifiques de Johns Hopkins Medicine affirment avoir réussi à fournir des paquets de code génétique de taille nanométrique appelés microARN pour traiter les tumeurs cérébrales humaines implantées chez la souris. Le contenu des très petits contenants a été conçu pour cibler les cellules souches cancéreuses, une sorte de "graine" cellulaire qui produit d'innombrables descendants et constitue une barrière implacable pour débarrasser le cerveau des cellules malignes.
Les résultats de leurs expériences ont été publiés en ligne le 21 juin dans Lettres nano .
"Le cancer du cerveau est l'un des cancers les mieux compris en termes de constitution génétique, mais nous devons encore développer un bon traitement pour cela, " dit John Laterra, MARYLAND., Doctorat., professeur de neurologie, l'oncologie et les neurosciences à l'École de médecine de l'Université Johns Hopkins et chercheur à l'Institut Kennedy Krieger. "La résilience des cellules souches cancéreuses et la barrière hémato-encéphalique sont des obstacles majeurs."
Le sang qui pénètre dans le cerveau est filtré à travers une série de vaisseaux qui agissent comme une barrière protectrice. Mais cette barrière hémato-encéphalique bloque les médicaments moléculaires qui ont le potentiel de révolutionner le traitement du cancer du cerveau en ciblant les cellules souches cancéreuses, dit Laterra.
« Pour moderniser les traitements des tumeurs cérébrales, nous avons besoin d'outils et de méthodes qui contournent la barrière hémato-encéphalique, " dit Jordan Green, Doctorat., professeur de génie biomédical, ophtalmologie, oncologie, neurochirurgie, science et ingénierie des matériaux et ingénierie chimique et biomoléculaire à la faculté de médecine de l'Université Johns Hopkins. "Nous avons besoin d'une technologie pour administrer en toute sécurité et efficacement des médicaments génétiques sensibles directement aux tumeurs sans endommager les tissus normaux."
Un cas d'espèce, Vert dit, est le glioblastome, la forme de cancer du cerveau que combat le sénateur de l'Arizona John McCain, qui nécessite souvent des interventions chirurgicales répétées. Les médecins enlèvent le tissu tumoral cérébral qu'ils peuvent voir, mais la malignité revient souvent rapidement, dit Laterra. La plupart des patients atteints de glioblastome vivent moins de deux ans après le diagnostic.
Les scientifiques soupçonnent depuis longtemps que les cellules souches cancéreuses sont à l'origine du retour et de la propagation du glioblastome et d'autres cancers. Ces cellules souches donnent naissance à d'autres cellules cancéreuses et, s'ils échappent au couteau du chirurgien, peut conduire à une tumeur entièrement nouvelle.
Laterra et Vert, qui sont membres du Johns Hopkins Kimmel Cancer Center, a conçu un moyen d'administrer efficacement de très petits paquets de microARN dans des tumeurs cérébrales établies. Les microARN ciblent les cellules souches du cancer du cerveau pour arrêter leur capacité à se propager et à maintenir la croissance tumorale.
Les sachets sont faits de plastique biodégradable similaire au matériau utilisé pour les sutures chirurgicales et qui se dégrade avec le temps. Ils sont 1, 000 fois plus petit que la largeur d'un cheveu humain et typique de la taille et de la forme des composants naturels que les cellules utilisent pour communiquer. Lorsque les cellules cancéreuses engloutissent les paquets, ils se séparent et libèrent leur « charge utile » de microARN spécifiquement là où les microARN doivent agir dans les cellules cancéreuses.
Enfermés dans le nanopaquet se trouvent des microARN qui se lient spécifiquement aux ARN messagers liés à deux gènes :HMGA1 et DNMT, qui fonctionnent ensemble pour réguler les programmes d'expression génique dans les cellules.
Lorsque les microARN se lient à ces ARN messagers, ils bloquent leurs capacités de fabrication de protéines et désactivent les programmes qui déterminent les caractéristiques souches des cellules cancéreuses. Sans leurs propriétés de tige, les cellules cancéreuses sont plus différenciées, ils perdent leur capacité à propager des tumeurs, et ils peuvent être plus sensibles aux radiations et aux médicaments.
Pour leurs expériences, les scientifiques de Johns Hopkins ont implanté des cellules de glioblastome humain dans 18 souris. Pour imiter le défi clinique du traitement d'une tumeur existante, les scientifiques ont attendu 45 jours avant de traiter les animaux pour s'assurer qu'ils avaient des tumeurs bien formées. La moitié des animaux ont reçu des infusions des nanopaquets contenant des microARN actifs directement dans leurs tumeurs cérébrales, et l'autre moitié a reçu des nanopaquets contenant des microARN inactifs. Pour isoler l'effet des nanoparticules, les scientifiques ont utilisé des souris élevées sans cellules T du système immunitaire qui ciblent les cellules cancéreuses.
Cinq des neuf souris recevant des microARN inactifs (témoins) sont mortes dans les deux mois, et le reste des souris témoins sont morts dans les 90 jours. Trois des neuf souris recevant des microARN actifs ont duré jusqu'à 80 jours, and six lived to 133 days. Those six were humanely euthanized, and isolated mouse brains were examined for the presence of tumors.
All of the control mice had large tumors in their brains when they died. Four of the mice that received active microRNAs and lived to 133 days had no tumors, and two had small ones.
Green says that many genetic medicines are designed to target one gene. The type of nanoparticles the Johns Hopkins team used in this study can encapsulate multiple types of microRNAs to target multiple gene networks.
When the brain cancer stem cells internalize the nanoparticle and transition to a non-stem-cell state, Laterra says, clinicians could exploit that condition, and give radiation or other drugs to kill the now-vulnerable cells.
Green says scientific teams elsewhere are developing microRNA packets using lipid-based materials, and some standard chemotherapy is delivered in a fatty nanoparticle called a liposome.
Green and Laterra say the nanoparticles in their study are able to permeate the entire tumor because rodent brains are small. Humans, with bigger brains, may need a pump and catheter to funnel nanoparticles throughout the brain.
The Johns Hopkins team is working to scale up development of its nanoparticles and standardize their stability and quality before applying for permission to begin clinical trials on people.