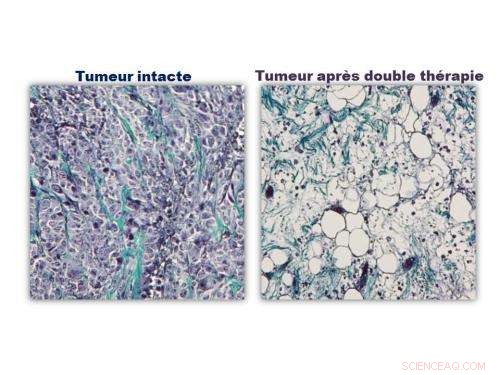
Coloration trichrome de Masson :les noyaux cellulaires sont bleu-noir, les cytoplasmes (corps cellulaires) sont mauves et les fibres de collagène sont vertes. © Riccardo Di Corato - laboratoire MSC. Crédit :CNRS/Université Paris Diderot
En combinant, dans un liposome, des nanoparticules magnétiques et des photosensibilisateurs activés simultanément et à distance par des stimuli physiques externes (un champ magnétique et de la lumière), des scientifiques du Laboratoire Matière et Systèmes Complexes (CNRS/Université Paris Diderot) et du Laboratoire Physicochimie des Electrolytes et Nanosystèmes Interfaciaux (CNRS/UPMC), obtenu une régression tumorale totale chez la souris. Non toxiques lorsqu'ils ne sont pas activés, de telles thérapies peuvent également permettre une réduction des effets indésirables. Ces résultats, qui démontrent l'importance des traitements multiples, ont été publiés dans ACS Nano le 24 mars 2015.
L'une des stratégies employées pour limiter les effets indésirables des thérapies anticancéreuses est le développement de systèmes de nanosupports capables de véhiculer des ingrédients actifs vers des cellules tumorales cibles. On parle de thérapies « physiques » lorsque les substances actives, molécules ou nanoparticules, peut être activé à distance par des stimuli physiques externes - dans ce cas par la lumière ou un champ magnétique. Dans ce contexte, l'équipe d'étude a développé un nouveau type de support qui combine la photosensibilité et le magnétisme. Pour y parvenir, ils ont d'abord encapsulé des nanoparticules magnétiques dans le compartiment interne d'un liposome en quantité suffisante pour le rendre ultra-magnétique, avant d'incorporer des photosensibilisateurs dans sa bicouche lipidique, tout en préservant une taille optimale pour la circulation dans le sang.
Ces liposomes, contenant des nanoparticules magnétiques et des photosensibilisateurs, ont été injectés directement dans la tumeur dans le modèle murin. Les scientifiques ont ainsi combiné deux techniques pour parvenir à une destruction complète des cellules cancéreuses. Le premier, hyperthermie magnétique, consiste à exciter les nanoparticules avec un champ magnétique pour élever la température de la tumeur et la détruire. La seconde méthode, la thérapie photodynamique, est rendu possible par les photosensibilisateurs, lequel, lorsqu'il est activé, libèrent des espèces réactives de l'oxygène qui sont toxiques pour les cellules tumorales. Ces deux kinésithérapies agissent en synergie sur l'activité des protéines impliquées dans l'apoptose, ou mort cellulaire programmée. Leur association induit donc une régression totale de la tumeur, alors qu'une seule thérapie n'est pas en mesure d'arrêter sa croissance.
Pour l'équipe de recherche, l'étape suivante consiste à exploiter les « autres » propriétés magnétiques des liposomes afin d'améliorer le traitement :les nanoparticules sont en effet visibles en IRM et peuvent être déplacées à l'aide d'aimants. Après une injection dans la circulation sanguine, il deviendrait donc possible d'utiliser les aimants pour cibler les liposomes vers les tumeurs, tout en cartographiant leur destination finale par IRM.