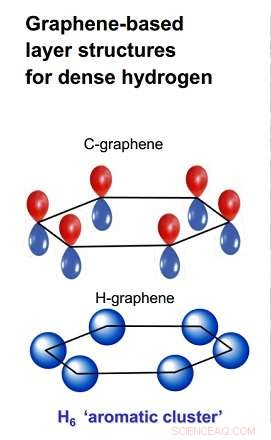
Une comparaison du graphène composé de carbone avec une structure similaire à base d'hydrogène synthétisée par les scientifiques de Carnegie. Crédit:Ivan Naumov et Russell Hemley de Carneige
De nouveaux travaux d'Ivan Naumov et Russell Hemley de Carnegie explorent la chimie sous-jacente à certaines observations récentes surprenantes sur l'hydrogène, et révèle des parallèles remarquables entre l'hydrogène et le graphène sous des pressions extrêmes. Leur travail fait la couverture du numéro de décembre de Comptes de la recherche chimique .
L'hydrogène est l'élément le plus abondant du cosmos. Avec un seul électron par atome, c'est d'une simplicité trompeuse. Par conséquent, l'hydrogène a été un terrain d'essai pour les théories de la liaison chimique depuis la naissance de la mécanique quantique il y a un siècle. Comprendre la nature des liaisons chimiques dans les environnements extrêmes est crucial pour élargir notre compréhension de la matière dans le large éventail de conditions présentes dans l'univers.
Observer le comportement de l'hydrogène sous de très hautes pressions a été un grand défi pour les chercheurs. Mais récemment, des équipes ont pu observer qu'à des pressions de 2 à 3,5 millions de fois la pression atmosphérique normale, il se transforme en une structure inattendue constituée de feuilles stratifiées, plutôt qu'un métal compacté comme cela avait été prédit il y a de nombreuses années.
Ces feuilles d'hydrogène ressemblent au graphène composé de carbone. Les couches de graphène sont chacune constituées d'une structure en nid d'abeilles constituée d'anneaux de carbone à six atomes. Ce graphène de carbone conventionnel, synthétisé pour la première fois il y a une dizaine d'années, est très léger, mais incroyablement fort, et conduit la chaleur et l'électricité très efficacement. Ces propriétés promettent une technologie révolutionnaire, y compris l'électronique optique avancée pour les écrans, cellules photovoltaïques à haut rendement, et des batteries améliorées et d'autres dispositifs de stockage d'énergie.
Les nouveaux travaux de Naumov et Hemley montrent que la stabilité de la structure inhabituelle de l'hydrogène découle de la stabilité intrinsèque de ses cycles d'hydrogène. Ces anneaux se forment à cause de ce qu'on appelle l'aromaticité, ce qui est bien compris dans les molécules carbonées comme le benzène, ainsi que dans le graphène. Les structures aromatiques prennent une forme annulaire qui peut être considérée comme une alternance de carbones à liaison simple et double. Mais ce qui se passe réellement, c'est que les électrons qui composent ces liaisons théoriquement alternées se délocalisent et flottent dans un cercle partagé autour de l'intérieur de l'anneau, stabilité croissante.
L'étude de Naumov et Hemley indique également que l'hydrogène devient initialement un métal sombre peu conducteur comme le graphite au lieu d'un métal brillant conventionnel et un bon conducteur, comme cela a été suggéré à l'origine dans des calculs théoriques remontant aux années 1930 en utilisant les premiers modèles de mécanique quantique pour les solides.
Bien que la découverte de ce caractère en couches d'hydrogène dense ait été une surprise pour beaucoup, les chimistes il y a 30 ans, avant la découverte du graphène, avaient prédit la structure sur la base de simples considérations chimiques. Leurs travaux sont validés et prolongés par les nouvelles découvertes.
"Globalement, nos résultats indiquent que la liaison chimique se produit dans un éventail de conditions beaucoup plus large que ce que les gens avaient envisagé auparavant. Cependant, les effets structurels de cette liaison chimique dans des conditions extrêmes peuvent être très différents de ceux observés dans les conditions ordinaires qui nous sont familières, " a déclaré Hemley.