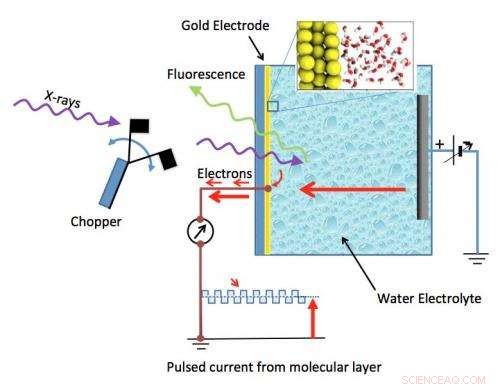
Schéma de la cellule électrochimique - une membrane en nitrure de silicium (Si3N4) sépare le liquide de la région sous vide de la source de rayons X ; une électrode en or à couche mince de 20 nm est déposée sur le côté liquide de la membrane. La détection de l'absorption des rayons X se fait par émission de fluorescence du côté du vide ou par émission d'électrons au niveau de l'électrode en or. Crédit :Berkeley Lab
Lorsqu'un matériau solide est immergé dans un liquide, le liquide immédiatement à côté de sa surface diffère de celui du liquide en vrac au niveau moléculaire. Cette couche interfaciale est essentielle à notre compréhension d'un ensemble diversifié de phénomènes allant de la biologie à la science des matériaux. Lorsque la surface solide est chargée, tout comme une électrode dans une batterie de travail, il peut entraîner d'autres changements dans le liquide interfacial. Cependant, élucider la structure moléculaire à l'interface solide-liquide dans ces conditions s'est avéré difficile.
Maintenant, pour la première fois, des chercheurs du laboratoire national Lawrence Berkeley (Berkeley Lab) du département américain de l'Énergie (DOE) ont observé la structure moléculaire de l'eau liquide à une surface d'or dans différentes conditions de charge.
Michel Salmeron, chercheur principal à la division des sciences des matériaux (MSD) du Berkeley Lab et professeur au département des sciences et de l'ingénierie des matériaux de l'UC Berkeley, explique cela dans le contexte d'une batterie. "Sur une surface d'électrode, l'accumulation de charges électriques, entraîné par une différence de potentiel (ou tension), produit un champ électrique puissant qui entraîne des réarrangements moléculaires dans l'électrolyte à côté de l'électrode."
Les chercheurs de Berkeley Lab ont développé une méthode non seulement pour regarder les molécules à côté de la surface de l'électrode, mais pour déterminer leur disposition change en fonction de la tension.
Avec de l'or comme électrode chimiquement inerte, et de l'eau légèrement salée comme électrolyte, Salmeron et ses collègues ont utilisé une nouvelle version de la spectroscopie d'absorption des rayons X (XAS) pour sonder l'interface et montrer comment les molécules interfaciales sont disposées.
XAS lui-même n'est pas nouveau. Dans ce processus, un matériau absorbe les photons de rayons X à un taux spécifique en fonction de l'énergie des photons. Un tracé de l'intensité d'absorption en fonction de l'énergie est appelé un spectre qui, comme une empreinte digitale, est caractéristique d'une molécule de matériau donnée et de son état chimique. Nos yeux reconnaissent de nombreux matériaux par leurs couleurs caractéristiques, qui sont liés à leurs spectres d'absorption de la lumière visible. Les photons de rayons X utilisés dans cette étude ont des énergies environ 250 fois supérieures à celles de la lumière visible et sont générés à la source lumineuse avancée (ALS) de Berkeley Lab.
Les mesures XAS typiques sont effectuées dans des conditions de vide, comme les rayons X sont facilement absorbés par la matière, même les molécules d'azote dans l'air. Mais les liquides s'évaporent rapidement dans le vide. En utilisant un très fin (100 nm, ou un dixième de micromètre) fenêtre transparente aux rayons X, avec une fine couche d'or (20 nm), sur un porte-échantillon liquide scellé, l'équipe du Berkeley Lab a pu exposer des molécules d'eau dans le liquide aux rayons X et collecter leurs spectres.
Lors de l'absorption d'un photon de rayon X, la molécule d'eau excitée peut cracher (émettre) soit des particules chargées (électrons) soit de la lumière (photons). La quantité d'émission de photons, ou fluorescence, est un indicateur du nombre de photons de rayons X qui ont été absorbés. Cependant, les rayons X fluorescents peuvent être détectés à partir de molécules allant de celles à la surface de l'or à celles en profondeur (micromètres) à l'intérieur du liquide loin de l'influence de la surface de l'or, et ceux-ci dominent le spectre mesuré.
"Nous ne nous intéressons vraiment qu'à une région interfaciale à l'échelle nanométrique, et en regardant le signal des photons de fluorescence, nous ne pouvons pas faire la différence entre l'interface et les molécules d'électrolyte intérieures, " dit Salmeron.
Le défi était donc de collecter un signal qui serait dominé par la région interfaciale. L'équipe a accompli cela en mesurant les émissions d'électrons, car les électrons émis par les molécules d'eau excitées par les rayons X ne parcourent que des distances nanométriques à travers la matière. Les électrons arrivant à la surface de l'électrode en or peuvent être détectés comme un courant électrique traversant un fil qui y est attaché. Cela évite la confusion avec les signaux de l'électrolyte intérieur car les électrons émis par les molécules intérieures ne voyagent pas assez loin pour être détectés.
Il y a un problème supplémentaire qui se pose lors de l'étude des liquides en contact avec des électrodes de travail car ils transportent un courant constant comme dans les batteries et autres systèmes électrochimiques. Alors que les électrons émis par les molécules voisines sont effectivement détectables, cette contribution au courant est éclipsée par le courant "faradique" normal de la batterie à des tensions finies. Lors de la mesure du courant hors de l'électrode, il est essentiel de déterminer quelle partie est due aux rayons X et laquelle est due au courant normal de la batterie.
Pour surmonter ce problème, les chercheurs ont pulsé les rayons X entrants du synchrotron à une fréquence connue. La contribution de courant résultant de l'émission d'électrons par les molécules interfaciales est donc également pulsée, et les instruments peuvent séparer ce courant modulé en nanoampères du courant faradique principal.
Ces expériences donnent lieu à des courbes d'absorption par rapport à l'énergie des rayons X (spectres) qui reflètent la façon dont les molécules d'eau situées à quelques nanomètres de la surface de l'or absorbent les rayons X. Pour traduire cette information en structure moléculaire, une technique d'analyse théorique sophistiquée est nécessaire.
David Prendergast, chercheur au sein de la Molecular Foundry et chercheur au Joint Center for Energy Storage Research (JCESR), a développé des techniques informatiques qui permettent à son équipe d'accomplir cette traduction.
En utilisant les installations de superordinateurs du Centre national de calcul scientifique de la recherche énergétique de Berkeley Lab (NERSC), il a mené de grandes simulations de dynamique moléculaire de l'interface or-eau, puis a prédit les spectres d'absorption des rayons X de structures représentatives à partir de ces simulations.
"Ce sont des calculs de premier principe, " explique Prendergast. " Nous ne dictons pas la chimie :nous choisissons simplement quels éléments atomiques sont présents et combien d'atomes. C'est ça. La chimie est le résultat du calcul."
Il s'avère que pour une surface d'or neutre, un nombre important de molécules d'eau (H2O) à côté de la surface de l'or s'orientent avec des atomes d'hydrogène (H) pointant vers l'or. Les molécules d'eau sont liées entre elles par des liaisons hydrogène, qui orientent les atomes H légèrement chargés positivement dans chaque molécule vers les atomes d'oxygène (O) légèrement chargés négativement des molécules voisines. Ce réseau de liaisons hydrogène est ce qui maintient les molécules d'eau ensemble pour former un liquide dans des conditions de température et de pression que nous considérons confortables en tant qu'êtres humains. Il est peut-être surprenant que la surface de l'or inerte puisse inciter un nombre important de molécules d'eau à ne pas se lier les unes aux autres, mais à se lier à l'or à la place. Ce nombre est augmenté lorsque l'or est chargé négativement et attire donc les atomes H les plus positifs. Par ailleurs, les ions d'or chargés positivement amènent les molécules d'eau à éloigner leurs atomes H de l'or, qui renforce le réseau de liaisons hydrogène du liquide interfacial.
« C'est la principale chose que nous savons sur la surface de l'électrode en or à partir des spectres d'absorption des rayons X :combien de molécules d'eau sont inclinées d'une manière ou d'une autre, et si leurs liaisons hydrogène sont rompues ou non, " conclut Salmeron. " L'eau à côté de l'électrode a une structure moléculaire différente de celle qu'elle aurait en l'absence de l'électrode. "
Il y a quelques choses subtiles qui sont très importantes, note Prendergast. D'abord, la forme des spectres d'absorption change en fonction de l'évolution de la tension. Puisque les spectres mesurés concordent avec les calculs, on peut tirer des conclusions sur la structure moléculaire de l'interface liquide en fonction de la tension. La seconde est que dans les calculs, le changement dans la structure de l'eau est limité aux deux premières couches moléculaires au-dessus de la surface et ces deux couches ne s'étendent que sur environ 1 nanomètre. Observer toute différence dans les spectres expérimentaux avec une tension variable signifie que les mesures sont sensibles à une échelle de longueur plus courte qu'on ne le pensait possible.
"On pensait que la sensibilité était de quelques dizaines de nanomètres, mais il s'avère être subnanométrique, " dit Prendergast. " C'est spectaculaire ! "
Cette étude, qui est rapporté dans Science dans un article intitulé "La structure de l'eau interfaciale sur des électrodes d'or étudiées par spectroscopie d'absorption des rayons X, " marque la première fois que la communauté scientifique montre une sensibilité aussi élevée dans un environnement in-situ dans des conditions d'électrode de travail.