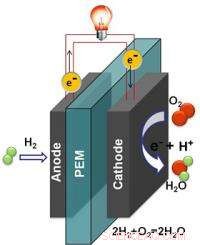
Les piles à combustible fonctionnent en décomposant électrochimiquement le carburant au lieu de le brûler, convertir directement l'énergie en électricité.
En quête d'efficacité, des piles à combustible rentables et commercialement viables, des scientifiques de l'Energy Materials Center de l'Université Cornell ont découvert une combinaison catalyseur et catalyseur-support qui pourrait rendre les piles à combustible plus stables, conk-out gratuit, peu coûteux et plus résistant à l'empoisonnement au monoxyde de carbone.
La recherche, « Pt/Ti hautement stable et tolérant au CO
Les piles à combustible à hydrogène offrent une alternative intéressante aux voitures à essence :elles ont le potentiel d'alimenter des véhicules sur de longues distances en utilisant l'hydrogène comme carburant, atténuer la production de dioxyde de carbone et n'émettre que de la vapeur d'eau.
Cependant, les piles à combustible nécessitent généralement de l'hydrogène très pur pour fonctionner. Cela signifie que les carburants conventionnels doivent être débarrassés du monoxyde de carbone - un processus trop coûteux pour rendre les piles à combustible commercialement viables.
Les piles à combustible fonctionnent en décomposant électrochimiquement le carburant au lieu de le brûler, convertir directement l'énergie en électricité.
Le problème est que le platine et les alliages platine/ruthénium, qui sont souvent utilisés comme catalyseurs dans les piles à combustible PEM (membrane échangeuse de protons), sont coûteux et facilement rendus inefficaces par une exposition à des niveaux même faibles de monoxyde de carbone.
Pour créer un système de catalyseur qui peut tolérer plus de monoxyde de carbone, Abruna, DiSalvo et ses collègues ont déposé des nanoparticules de platine sur un support en oxyde de titane additionné de tungstène pour augmenter sa conductivité électrique.
Leurs recherches montrent que le nouveau matériau fonctionne avec un carburant qui contient jusqu'à 2% de monoxyde de carbone - un niveau qui est environ 2000 fois celui qui empoisonne généralement le platine pur. Aussi, le matériau est plus stable et moins cher que le platine pur. Avec le nouveau catalyseur, dit Abruna, "vous pouvez utiliser de l'hydrogène beaucoup moins propre, et c'est plus rentable parce que l'hydrogène dérivé du pétrole a une teneur très élevée en monoxyde de carbone. Vous devez éliminer le monoxyde de carbone et cela coûte très cher."
Les chercheurs se préparent maintenant à tester le catalyseur dans de vraies piles à combustible. "Jusque là, les indications sont très bonnes, " a déclaré Abruna.
Dans des expériences préliminaires comparant les performances du nouveau matériau avec du platine pur, il ajouta, la cellule de platine a été facilement empoisonnée par le monoxyde de carbone et s'est éteinte tôt. Abruña a déclaré:"Mais le nôtre fonctionnait toujours comme un champion."