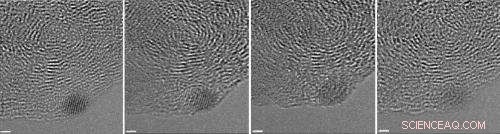
Une série d'images montre un petit nanodiamant (la tache sombre dans le coin inférieur droit) redevenant anthracite. Des scientifiques de l'Université Rice ont vu des nanodiamants se former dans le charbon hydrogéné lorsqu'ils sont touchés par le faisceau d'électrons utilisé dans les microscopes électroniques à transmission haute résolution. Mais des diamants plus petits comme celui-ci se sont dégradés avec les images suivantes. La barre d'échelle est de 1 nanomètre. Crédit:Billups Lab/Rice University
(Phys.org) —Les images prises par les scientifiques de l'Université Rice montrent que certains diamants ne sont pas éternels. Les chercheurs de Rice à l'origine d'une nouvelle étude expliquant la création de nanodiamants dans le charbon traité montrent également que certains diamants microscopiques ne durent que quelques secondes avant de redevenir des formes de carbone moins structurées sous l'impact d'un faisceau d'électrons.
La recherche du chimiste de Rice Ed Billups et de ses collègues apparaît dans l'American Chemical Society's Journal des lettres de chimie physique .
Billups et Yanqiu Sun, un ancien chercheur postdoctoral dans son laboratoire, a été témoin de l'effet intéressant en travaillant sur des moyens de réduire chimiquement le carbone du charbon anthracite et de le rendre soluble. Ils ont d'abord remarqué la formation de nanodiamants au milieu de l'amorphe, couches de graphite imprégnées d'hydrogène.
C'est arrivé, ils ont découvert, quand ils ont pris des gros plans du charbon avec un microscope électronique, qui tire un faisceau d'électrons au point d'intérêt. De façon inattendue, l'apport d'énergie a figé des amas d'atomes de carbone hydrogénés, dont certains ont pris la structure en treillis des nanodiamants.
"Le faisceau est très puissant, " a déclaré Billups. " Pour éliminer des atomes d'hydrogène de quelque chose, il faut une énorme quantité d'énergie. "

Les taches sombres sur ces images sont des nanodiamants formés dans du charbon anthracite hydrogéné lorsqu'ils sont touchés par les faisceaux d'un microscope électronique, selon des chercheurs de l'Université Rice. Crédit:Billups Lab/Rice University
Même sans le genre de pression nécessaire pour fabriquer des diamants à grande échelle, l'énergie a renversé des atomes d'hydrogène libres pour provoquer une réaction en chaîne entre les couches de graphite dans le charbon qui a abouti à des diamants entre 2 et 10 nanomètres de large.
Mais les plus "nano" des nanodiamants ont été vus s'estomper sous la puissance du faisceau d'électrons dans une succession d'images prises en 30 secondes.
"Les petits diamants ne sont pas stables et ils retournent à la matière première, l'anthracite, " a déclaré Billups.
Billups s'est tourné vers le physicien théoricien Rice Boris Yakobson et ses collègues de l'Institut technologique pour les matériaux superdurs et nouveaux en carbone à Moscou pour expliquer ce que les chimistes ont vu. Yakobson, Pavel Sorokin et Alexander Kvashnin avaient déjà mis au point un graphique, appelé diagramme de phases, qui montrait comment des films de diamant minces pouvaient être fabriqués sans pression massive.
Ils ont utilisé des calculs similaires pour montrer comment des nanodiamants pouvaient se former dans l'anthracite traité et le charbon subbitumineux. Dans ce cas, le faisceau du microscope électronique détache les atomes d'hydrogène des couches de carbone. Ensuite, les liaisons pendantes compensent en se connectant à une couche de carbone adjacente, qui est invité à se connecter à la couche suivante. La réaction compresse les atomes dans une matrice caractéristique du diamant jusqu'à ce que la pression force le processus à s'arrêter.
Naturel, les diamants à grande échelle nécessitent des pressions et des températures extrêmes pour se former, mais le diagramme de phase devrait être reconsidéré pour les nanodiamants, les chercheurs ont dit.
"Il existe une fenêtre de stabilité pour les diamants dans la plage de 19 à 52 angströms (dixièmes de nanomètre), au-delà de laquelle le graphite est plus stable, " a déclaré Billups. Des nanodiamants stables jusqu'à 20 nanomètres de taille peuvent être formés dans de l'anthracite hydrogéné, ils ont trouvé, bien que les plus petits nanodiamants soient instables sous un rayonnement continu de faisceau d'électrons.
Billups a noté que des expériences ultérieures de faisceau d'électrons avec de l'anthracite vierge n'ont formé aucun diamant, tandis que des tests avec des infusions d'hydrogène moins robustes ont conduit à des régions avec des "franges en forme d'oignon" de carbone graphitique, mais pas de diamants entièrement formés. Les deux expériences ont confirmé le besoin de suffisamment d'hydrogène pour former des nanodiamants.
Kvashnin est un ancien étudiant invité à Rice et un étudiant diplômé de l'Institut de physique et de technologie de Moscou (MIPT). Sorokin occupe des postes au MIPT et à l'Université nationale des sciences et technologies, Moscou. Yakobson est professeur Karl F. Hasselmann de Rice en génie mécanique et science des matériaux, professeur de chimie et membre du Richard E. Smalley Institute for Nanoscale Science and Technology. Billups est professeur de chimie à Rice.