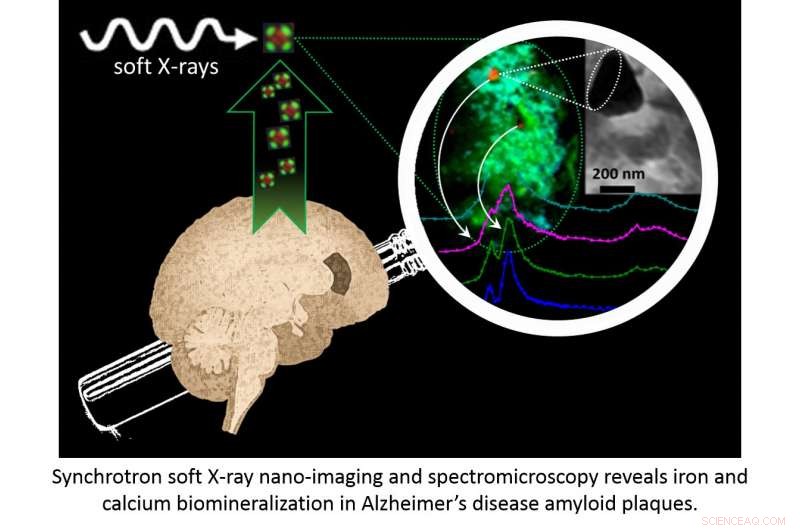
Crédit :Source de lumière diamant
Spectromicroscopie à rayons X à la ligne de lumière de Microscopie à Rayons X à Balayage (I08), ici au Diamant, a été utilisé pour localiser des composés de fer et de calcium chimiquement réduits dans des plaques de protéines dérivées de cerveaux de patients atteints de la maladie d'Alzheimer. L'étude, Publié dans Nanoéchelle , a mis en lumière la manière dont les espèces métalliques contribuent à la pathogenèse de la maladie d'Alzheimer et pourraient aider à orienter les thérapies futures.
La maladie d'Alzheimer est une maladie neurodégénérative associée à la démence et à une espérance de vie réduite. La maladie se caractérise par la formation de plaques de protéines et d'enchevêtrements dans le cerveau qui altèrent le fonctionnement. En plus des plaques de protéines, l'homéostasie des ions métalliques perturbée est également liée à la pathogenèse, et les niveaux de fer en particulier sont élevés dans certaines régions du cerveau.
Une équipe de scientifiques ayant une longue histoire dans l'exploration de la biominéralisation dans le cerveau d'Alzheimer a entrepris de caractériser les espèces de fer associées aux plaques de protéines amyloïdes. Ils ont extrait des échantillons du cerveau de deux patients décédés atteints de la maladie d'Alzheimer et appliqué la spectromicroscopie à rayons X synchrotron pour différencier les phases d'oxyde de fer dans les échantillons.
Ils ont noté des preuves que la réduction chimique du fer, et en effet la formation d'un oxyde de fer magnétique appelé magnétite, qui ne se trouve pas couramment dans le cerveau humain, s'était produite lors de la formation de la plaque amyloïde, une découverte qui pourrait aider à éclairer les résultats des futures thérapies contre la maladie d'Alzheimer.
Espèces de fer réduites
La maladie d'Alzheimer est la forme la plus courante de démence, qui touche environ 850 personnes, 000 personnes au Royaume-Uni. La prévalence de la maladie d'Alzheimer devant augmenter au cours des prochaines décennies, et sans remède ni traitement, la recherche sur la pathogenèse de la maladie est vitale.
L'une des caractéristiques de la maladie d'Alzheimer est la formation de plaques amyloïdes. Ils surviennent via l'accumulation d'amyloïde-β, qui forme des dépôts insolubles dans le cerveau et altère son fonctionnement. Parallèlement à la formation de plaques, l'homéostasie des métaux est également perturbée. Les niveaux de fer sont augmentés dans plusieurs régions du cerveau d'Alzheimer et des concentrations élevées de formes de fer chimiquement réduites sont associées aux caractéristiques pathologiques de la maladie.
Une collaboration entre des scientifiques de l'Université de Keele, Université de Warwick, L'Université de Floride et l'Université du Texas à San Antonio ont entrepris d'étudier la relation entre les espèces réduites de fer et l'amyloïde-β. Cette équipe avait déjà une expérience dans l'étude des métaux dans le cerveau d'Alzheimer et leurs travaux sont étayés par l'hypothèse qu'il y avait plus de réduction chimique du fer que la normale lorsque l'amyloïde-β s'agrège.
« Nous voulions savoir comment le fer interagit avec la protéine amyloïde lorsqu'il forme les dépôts insolubles. Nous voulions examiner le matériel humain pour voir s'il existe des preuves du processus que nous voyons in vitro, " a expliqué le Dr Joanna Collingwood, Professeur agrégé à l'Université de Warwick et membre de l'équipe de recherche.
Noyaux de plaque amyloïde extraits
L'équipe a extrait des carottes de plaque amyloïde de deux patients décédés ayant reçu un diagnostic formel de la maladie d'Alzheimer. La microscopie à rayons X à transmission à balayage a été réalisée à l'Advanced Light Source (ALS) à Berkeley, USA et à la ligne I08 à Diamond. Une série d'images ont été prises à des énergies de photons couvrant un bord d'absorption pour produire une « pile », qui ont été utilisés pour déterminer l'état d'oxydation chimique des minéraux dans chaque région d'intérêt. Le dichroïsme circulaire magnétique à rayons X in situ (XMCD) a également été mené à I08 pour sonder l'état magnétique des espèces de fer, et confirment ainsi la présence des minéraux de fer magnétique.
Le Dr Collingwood a expliqué l'importance de l'I08 dans l'étude :« Nous devions pouvoir voir sur une échelle de longueur qui était pertinente pour les structures au sein des noyaux de la plaque amyloïde, qui nécessitait une ligne de lumière capable de travailler à des dizaines de nanomètres de résolution et pourrait nous permettre d'observer les métaux de transition. Nous avons pu collecter des informations sur les composants organiques en observant les caractéristiques spectrales de la teneur en protéines, puis en regardant les distributions de métaux associées à la matière organique. Cela nous a permis d'imager et d'analyser la matière organique et inorganique de la même région dans l'échantillon sans aucun type d'étiquetage. »
Production de radicaux libres
L'équipe a vu de nombreux types de formes réduites de fer dans les noyaux de plaque amyloïde extraits. Ils en ont déduit que la réduction chimique atypique du fer et l'augmentation du cycle redox dans le cerveau d'Alzheimer contribuaient à la pathogenèse de la maladie.
"Là où vous avez une réduction chimique du fer, cela offre la possibilité de produire catalytiquement des radicaux libres. Des dommages causés par les radicaux libres ont été signalés sur des sites d'agrégation amyloïde, la toxicité associée à l'amyloïde pourrait donc être due à la réduction du fer, " a expliqué le Dr Collingwood.
Curieusement, avec l'aide de XMCD, ils ont également vu une espèce magnétique inhabituelle de fer appelée magnétite à l'intérieur des plaques. Des observations ptychographiques à l'ALS ont indiqué que la magnétite de cet échantillon était biogénique, et non dérivé de sources industrielles telles que les polluants comme indiqué dans une autre étude récente.
L'équipe a ajouté à la base de connaissances de la pathologie d'Alzheimer en trouvant des preuves de calcium dans les plaques amyloïdes, et a démontré que plusieurs phases de calcium doivent coexister dans les plaques, quelque chose qui n'avait jamais été signalé auparavant.
La prochaine étape pour l'équipe est de regarder directement dans le tissu cérébral humain plutôt que d'extraire des noyaux de plaque amyloïde, et aussi pour explorer d'autres métaux de transition. Autre part, des essais cliniques avec des médicaments modificateurs du fer sont en cours pour la maladie d'Alzheimer, ce travail sera donc inestimable pour l'interprétation des résultats de ces essais.